你可能感兴趣的试题
平衡时,X.的转化率为20%
t ℃时,该反应的平衡常数为40
增大平衡后的体系压强, v正增大,v逆减小, 平衡向正反应方向移动
前2 min内,用Y.的变化量表示的平均反应速率v(Y)="0.03" mol·L-1·min-1
m>n 温度不变,压强增大,Y.的质量分数减少 Q.<0 体积不变,温度升高,平衡向逆反应方向移动
等压时,通入惰性气体,Z.的物质的量不变 等压时,通入Z.气体,容器内温度改变 等容时,通入惰性气体,反应速率不变 等容时,通入Z.气体,Y.的物质的量浓度增大
容器中发生的反应可表示为:3X(g)+Y(g)  2Z(g) 反应进行的前3 min内,用X.表示的反应速率 v(X)=0.3mol/(L·min) 保持其他条件不变,升高温度,反应的化学平衡常数K.减小 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
2Z(g) 反应进行的前3 min内,用X.表示的反应速率 v(X)=0.3mol/(L·min) 保持其他条件不变,升高温度,反应的化学平衡常数K.减小 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
达到平衡时,反应放出QKJ热量 反应一段时间后,X.与Y.的物质的量之比认为1:1 X.的体积分数不变,说明反应已达到平衡状态 达到平衡后,若向平衡体系中充入氦气,Z.的反应速率不变
(g)+B(g) 2C(g) ΔH1<0,X(g)+3Y(g)
2C(g) ΔH1<0,X(g)+3Y(g) 2Z(g) ΔH2>0。进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( ) A.恒压时,通入Z.气体,反应容器中温度升高 恒容时,通入惰性气体,各反应速率不变 恒容时,通入Z.气体,Y.的物质的量浓度增大 恒压时,通入惰性气体,C.的物质的量不变
2Z(g) ΔH2>0。进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( ) A.恒压时,通入Z.气体,反应容器中温度升高 恒容时,通入惰性气体,各反应速率不变 恒容时,通入Z.气体,Y.的物质的量浓度增大 恒压时,通入惰性气体,C.的物质的量不变
(g)+B(g) 2C(g) ΔH1<0,X(g)+3Y(g)
2C(g) ΔH1<0,X(g)+3Y(g) 2Z(g) ΔH2>0。进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( ) A.恒压时,通入Z.气体,反应容器中温度升高 恒容时,通入惰性气体,各反应速率不变 恒容时,通入Z.气体,Y.的物质的量浓度增大 恒压时,通入惰性气体,C.的物质的量不变
2Z(g) ΔH2>0。进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( ) A.恒压时,通入Z.气体,反应容器中温度升高 恒容时,通入惰性气体,各反应速率不变 恒容时,通入Z.气体,Y.的物质的量浓度增大 恒压时,通入惰性气体,C.的物质的量不变
平衡时,X.的转化率为20% t ℃时,该反应的平衡常数为40 增大平衡后的体系压强, v正增大,v逆减小,平衡向正反应方向移动 前2 min内,用Y.的变化量表示的平均反应速率v(Y) = 0.03 mol·L-1·min-1
容器中发生的反应可表示为:3X(g)+Y(g) 2Z(g)
2Z(g)
反应进行前3min内,用X.表示的反应速率v(X)=0.1mol/(L·min)
若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 保持其他条件不变,升高温度,化学平衡向逆反应方向移动
容器中发生的反应可表示为:3X(g)+Y(g) 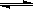 2Z(g)
2Z(g)
反应进行的前3 min内,用X.表示的反应速率 v(X)=0.3mol/(L·min)
保持其他条件不变,升高温度,反应的化学平衡常数K.增大
若改变反应条件,使反应进程如图3所示,则改变的条件可能是使用了催化剂
m>n 温度不变,压强增大,Y.的质量分数减少 Q.<0 体积不变,温度升高,平衡向逆反应方向移动
平衡时,X.的转化率为20% t ℃时,该反应的平衡常数为40 增大平衡后的体系压强, v正增大,v逆减小,平衡向正反应方向移动 前2 min内,用Y.的变化量表示的平均反应速率v(Y) = 0.03 mol·L-1·min-1
m>n Q<0 温度不变,压强增大,Y.的质量分数减少 体积不变,温度升高,平衡向逆反应方向移动
容器中发生的反应可表示为:3X(g)+Y(g) 
 2Z(g) 保持其他条件不变,升高温度,反应的化学平衡常数K.减小 反应进行的前3 min内,用X.表示的反应速率 v(X)=0.2mol·(L·min) −1 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂
2Z(g) 保持其他条件不变,升高温度,反应的化学平衡常数K.减小 反应进行的前3 min内,用X.表示的反应速率 v(X)=0.2mol·(L·min) −1 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂
容器中发生的反应可表示为:3X(g)+Y(g) 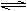
 2Z(g) 保持其他条件不变,升高温度,化学平衡向逆反应方向移动 反应进行前4 min内,用X.表示的反应速率 v(X)=0.075mol•(L•min) -1 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂
2Z(g) 保持其他条件不变,升高温度,化学平衡向逆反应方向移动 反应进行前4 min内,用X.表示的反应速率 v(X)=0.075mol•(L•min) -1 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂
等压时,通入惰性气体,Z.的物质的量不变 等压时,通入Z.气体,容器内温度改变 等容时,通入惰性气体,反应速率不变 等容时,通入Z.气体,Y.的物质的量浓度增大
升高温度,X.的体积分数减小 缩小体积,Y.的物质的量浓度不变 保持容器体积不变,充入1mol的稀有气体He,Z.的浓度不变 保持容器体积不变,充入2mol的Z(g),X.的体积分数增大

 2Z(g) 反应进行的前3 min内,用X.表示的反应速率 v(X)=0.3mol/(L·min) 保持其他条件不变,升高温度,反应的化学平衡常数K.减小 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
2Z(g) 反应进行的前3 min内,用X.表示的反应速率 v(X)=0.3mol/(L·min) 保持其他条件不变,升高温度,反应的化学平衡常数K.减小 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
 2C(g) ΔH1<0,X(g)+3Y(g)
2C(g) ΔH1<0,X(g)+3Y(g) 2Z(g) ΔH2>0。进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( ) A.恒压时,通入Z.气体,反应容器中温度升高 恒容时,通入惰性气体,各反应速率不变 恒容时,通入Z.气体,Y.的物质的量浓度增大 恒压时,通入惰性气体,C.的物质的量不变
2Z(g) ΔH2>0。进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( ) A.恒压时,通入Z.气体,反应容器中温度升高 恒容时,通入惰性气体,各反应速率不变 恒容时,通入Z.气体,Y.的物质的量浓度增大 恒压时,通入惰性气体,C.的物质的量不变
 2C(g) ΔH1<0,X(g)+3Y(g)
2C(g) ΔH1<0,X(g)+3Y(g) 2Z(g) ΔH2>0。进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( ) A.恒压时,通入Z.气体,反应容器中温度升高 恒容时,通入惰性气体,各反应速率不变 恒容时,通入Z.气体,Y.的物质的量浓度增大 恒压时,通入惰性气体,C.的物质的量不变
2Z(g) ΔH2>0。进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( ) A.恒压时,通入Z.气体,反应容器中温度升高 恒容时,通入惰性气体,各反应速率不变 恒容时,通入Z.气体,Y.的物质的量浓度增大 恒压时,通入惰性气体,C.的物质的量不变
 2Z(g)
2Z(g)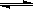 2Z(g)
2Z(g)
 2Z(g) 保持其他条件不变,升高温度,反应的化学平衡常数K.减小 反应进行的前3 min内,用X.表示的反应速率 v(X)=0.2mol·(L·min) −1 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂
2Z(g) 保持其他条件不变,升高温度,反应的化学平衡常数K.减小 反应进行的前3 min内,用X.表示的反应速率 v(X)=0.2mol·(L·min) −1 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂
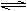
 2Z(g) 保持其他条件不变,升高温度,化学平衡向逆反应方向移动 反应进行前4 min内,用X.表示的反应速率 v(X)=0.075mol•(L•min) -1 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂
2Z(g) 保持其他条件不变,升高温度,化学平衡向逆反应方向移动 反应进行前4 min内,用X.表示的反应速率 v(X)=0.075mol•(L•min) -1 若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂