你可能感兴趣的试题
一定温度下,反应 MgCl2(l)===Mg(l)+Cl2(g)的ΔH.>0、ΔS. >0 放热反应的反应速率总是大于吸热反应的反应速率 在H2S溶液中,C.(H+)和C.(S2-)的比值为2:1 1 mol/L.和0.1 mol/L.的两瓶氨水中c(OH-)之比为10:1
一定温度下,反应MgCl2(1) ==Mg(1)+ Cl2(g)的 △H>0,△S>0 用pH均为12的NaOH溶液和氨水分别中和等物质的量的HCl,消耗氨水的v更大 N2(g)+3H2(g)  2NH3(g) (△H<0),当其他条件不变时,升高温度,H2的反应速率增大、转化率减小 对于乙酸与乙醇的酯化反应(△H.<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大
2NH3(g) (△H<0),当其他条件不变时,升高温度,H2的反应速率增大、转化率减小 对于乙酸与乙醇的酯化反应(△H.<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大
反应2A(g)+ (g)===3C(s)+D.(g)在一定条件下能自发进行,说明该反应的ΔH>0 B.常温下反应2Na2SO3(s)+O2(g)===2Na2SO4(s)能自发进行,则ΔH<0 反应2Mg(s)+CO2(g)===C(s)+2MgO(s)能自发进行,则该反应的ΔH>0 一定温度下,反应2NaCl(s)===2Na(s)+Cl2(g)的ΔH<0,ΔS>0
①②⑤ 只有②④ 只有①③ ①③⑤ 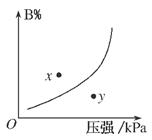
某反应的焓变△H>0,说明该反应为放热反应
酒精可用做燃料,说明酒精燃烧是放热反应
木炭需加热到一定温度时才燃烧,所以木炭燃烧是吸热反应
原电池中的盐桥只能通过电子,而离子无法通过
能与金属Al反应放出H2的溶液 加酚酞后显无色的溶液 pH=6的某溶液 c(H+)>c(OH—)的任意水溶液
一定大于92.0 kJ 一定等于92.0 kJ 一定小于92.0 kJ 不能确定
溶液中Na+浓度不变,有氧气生成 溶液中0H-浓度增大,有氢气生成 溶液中0H-浓度不变,溶液总质量增大 溶液中Na+数目减少,溶液总质量减少
一定大于92.0 kJ 一定等于92.0 kJ 一定小于92.0 kJ 不能确定
一定温度下,反应MgCl2(l) == Mg(l)+Cl2(g)的 ΔH>0 ΔS>0 凡是放热反应都是自发的,凡是吸热反应都是非自发的 常温下,水电解生成氢气和氧气,即常温下水的分解反应是自发反应 H2O(g)变成液态水,ΔS>0
反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的ΔH<0 反应CaCO3(s)=CaO(s)+CO2(g)在室温下不能自发进行,说明该反应ΔH<0 一定温度下,反应MgCl2(l)=Mg(l)+Cl2(g)的ΔH>0,ΔS>0 常温下,反应C.(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH>0
一定温度、常压 常温、__ 常温、常压 一定温度、一定压力

 2NH3(g) (△H<0),当其他条件不变时,升高温度,H2的反应速率增大、转化率减小 对于乙酸与乙醇的酯化反应(△H.<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大
2NH3(g) (△H<0),当其他条件不变时,升高温度,H2的反应速率增大、转化率减小 对于乙酸与乙醇的酯化反应(△H.<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大
