你可能感兴趣的试题
前50 s反应的平均速率v(PCl3)=0.0016 mol·L-1·s-1 其他条件不变,降低温度,平衡时c(PCl3)=0.09mol·L-1,则反应的△H.<0 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的转化率大于80% 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(逆)>v(正)
反应在前50 s的平均速率为v(PCl3)=0.0032 mol·L-1·s-1 保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol·L-1,则反应的△H<0 相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,达到平衡前 v(正)>v(逆) 相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,达到平衡时,PCl3的转化率 小于80%
10 min内,v (Cl2)=0.04 mol·L-1·min-1 当容器中Cl2为1.2 mol时,反应达到平衡 升高温度(T.1<T.2),反应的平衡常数减小,平衡时PCl3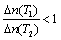 平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件再达平衡时,c(PCl5)<0.2 mol·L-1
平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件再达平衡时,c(PCl5)<0.2 mol·L-1
反应在前50 s的平均速率v(PCl3)=0.003 2 mol/(L·s) 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol/L,则反应的ΔH.<0 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的转化率小于80%
反应在前50 s的平均速率为v(PCl3)=0.0032 mol·L.-1·s-1 保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol·L.-1,则反应的△H.<0 相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,达到平衡前v(正)>v(逆) 相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,达到平衡时,PCl3的转化率小于80%
反应在前50 s的平均速率v(PCl3)= 0. 0032 mol·L-1·s-1 保持其他条件不变,升高温度,平衡时c(PCl3)= 0. 11 mol·L-1,则反应的△H<0 相同温度下,起始时向容器中充入1. 0 mol PCl5、0. 20 mol PCl3和0. 20 mol Cl2,反应达到平 衡前v(正)>v(逆) 相同温度下,起始时向容器中充入2. 0 mol PCl3和2. 0 mol Cl2,达到平衡时,PCl3的转化率 小于80%
反应在前50 s 的平均速率v(PCl3)= 0. 0032 mol·L-1·s-1 保持其他条件不变,升高温度,平衡时c(PCl3)= 0. 11 mol·L-1,则反应的H<0 相同温度下,起始时向容器中充入1. 0 mol PCl5、0. 20 mol PCl3 和0. 20 mol Cl2,反应达到平衡前v(正)>v(逆) 相同温度下,起始时向容器中充入2. 0 mol PCl3 和2. 0 mol Cl2,达到平衡时,PCl3 的转化率小于80%
反应在前50 s的平均速率v(PCl3)=0.003 2 mol·L-1·s-1 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L-1,则反应的ΔH.<0 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的转化率小于80%
0.4mol 大于0.2mol小于0.4mol 0.2mol 小于0.2mol
体系平衡时与反应起始时的压强之比为5∶6 反应在前50 s 的平均速率ν(PCl3)= 0. 0032 mol·L-1·s-1 相同温度下,起始时向容器中充入0.6mol PCl5、0. 20 mol PCl3 和0. 20 mol Cl2,反应达到平衡前ν(正)>ν(逆) 相同温度下,若起始时向容器中充入2. 0 mol PCl3 和2. 0 mol Cl2,达到平衡时,PCl3 的质量分数比上述平衡体系小
PCl5的分解率大于a% PCl5的分解率小于a% 达到平衡后正逆反应速率比原平衡状态时大 达到平衡后正逆反应速率比原平衡状态时小
10 min内,v(Cl2) = 0.04 mol/(L·min) 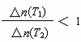 当容器中Cl2为1.2 mol时,反应达到平衡 若升高温度(T.1<T.2)时,该反应平衡常数减小,则平衡时PCl3的 平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L
当容器中Cl2为1.2 mol时,反应达到平衡 若升高温度(T.1<T.2)时,该反应平衡常数减小,则平衡时PCl3的 平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L
0~50 s内平均速率v(PCl3)= 0. 0032 mol·L-1·s-1 其他条件不变,升高温度,平衡时c(PCl3)= 0. 11 mol·L-1,则反应的△H<0 相同温度下,起始时向容器中充入1mol PCl5、0. 2 mol PCl3 和0. 2 mol Cl2,反应达到平衡前v(正)>v(逆) 相同温度下,起始时向容器中充入2 mol PCl3 、2 mol Cl2,达到平衡时PCl3 的转化率小于80%
反应在前50s的平均速率为v(PCl3)=0.0032mol/(L•s) 保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11mol/L,则反应的△H.<0 相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20mol Cl2,达到平衡前v(正)>v(逆) 相同温度下,起始时向容器中充入2.0mol PCl3、2.0mol Cl2,达到平衡时,PCl3的转化率小于80%
10 min内,v(Cl2)=0.04 mol/(L·min) 当容器中Cl2为1.2 mol时,反应达到平衡 升高温度,反应的平衡常数减小,则平衡时PCl3的转化率变大 平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L

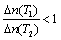 平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件再达平衡时,c(PCl5)<0.2 mol·L-1
平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件再达平衡时,c(PCl5)<0.2 mol·L-1
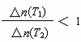 当容器中Cl2为1.2 mol时,反应达到平衡 若升高温度(T.1<T.2)时,该反应平衡常数减小,则平衡时PCl3的 平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L
当容器中Cl2为1.2 mol时,反应达到平衡 若升高温度(T.1<T.2)时,该反应平衡常数减小,则平衡时PCl3的 平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L