你可能感兴趣的试题
(g)+3B(g) 2C(g)达到平衡时,测得A., , 物质的量之比为2:2:1。若保持温度不变,以2:2:1的物质的量之比再充入A.B.C.,下列判断正确的是( ) A.平衡向逆反应方向移动B.平衡不会发生移动 C.C的质量分数增大 C的质量分数减小
2C(g)达到平衡时,测得A., , 物质的量之比为2:2:1。若保持温度不变,以2:2:1的物质的量之比再充入A.B.C.,下列判断正确的是( ) A.平衡向逆反应方向移动B.平衡不会发生移动 C.C的质量分数增大 C的质量分数减小
正反应的速率与逆反应的速率相同程度增加 只增加正反应的速率 只增加逆反应速率 正反应速率比逆速率增加得快
改变反应条件可以改变该反应的限度 达到平衡后,SO3、SO2、O2在密闭容器中共存 达到平衡后,反应停止,正、逆反应速率都等于零 SO3、SO2、O2的浓度保持不变,说明该可逆反应达到了平衡状态
加入少量W.,逆反应速率增大 当容器中气体压强不变时,反应达到平衡 升高温度,平衡逆向移动 改变条件,又达新平衡,此时上述反应的平衡常数K.值一定增大
可逆反应在一定条件下可建立化学平衡状态
处于化学平衡状态的可逆反应:v正=v逆≠0
可逆反应建立化学平衡时,与反应的起始方向无关,与反应物的起始浓度大小无关
一定条件下,可逆反应达到平衡时,反应混合物中各组分的浓度保持不变
可逆反应达到平衡的重要特征是各物质的反应速率相等。 在可逆反应里,正反应的速率是正值,逆反应的速率是负值。 对于H2+I2  2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
N2、H2、NH3在密闭容器中共存 N2、H2、NH3的浓度不再变化 N2、H2、NH3的浓度相等 正、逆反应速率都等于零
N2、H2、NH3的浓度不再变化 N2、H2、NH3的浓度相等 N2、H2、NH3在密闭容器中共存 反应停止,正、逆反应速率都等于零
不同的可逆反应,反应物的性质不同,平衡常数是相等的 对可逆反应来说,平衡常数越大,表示反应达到平衡时生成物浓度和反应物浓度的比值越大 对于同一个可逆反应,在不同的温度下,平衡常数有相同的数值 对可逆反应来说,平衡常数越大,表示反应完成的程度越小,物质的转化率越大
当可逆反应达到平衡状态时,v正 = v逆 = 0 当可逆反应达到平衡状态时,每种成分的质量分数保持不变 对于已达平衡的可逆反应,延长反应时间能提高反应物的转化率 对于已达平衡的可逆反应,改变外界条件时其平衡状态不会改变
(g)+B(g)  2C(g),可以判断达到化学平衡状态的是( ) A. 体系压强不变 单位时间消耗n molA,同时生成2nmolC A.的转化率不变 容器内气体密度不变
2C(g),可以判断达到化学平衡状态的是( ) A. 体系压强不变 单位时间消耗n molA,同时生成2nmolC A.的转化率不变 容器内气体密度不变
加入少量W.,逆反应速率增大 当容器中气体压强不变时,反应达到平衡 平衡后,加入X.,上述反应的△H.增大 升高温度,平衡正向移动
在同一条件下,对于一个可逆反应体系,当正反应速度大于逆反应速度时,此反应体系达到化学平衡 在同一条件下,对于一个可逆反应体系,当正反应速度小于逆反应速度时,此反应体系达到化学平衡 在同一条件下,对于一个可逆反应体系,当正反应速度等于逆反应速度时,此反应体系达到化学平衡
和1 mol ,发生可逆反应 3A(g)+2B(s) 2C(g)+D.(g) △H.=-a kJ/mol。5 min后达平衡,测得容器中n =0.8 mol。则下列说法正确的是( ) A.3vA.=2vC.=0.16 mol/(L·min) B.该可逆反应达平衡后,放出0.8a kJ的热能(假设化学能全转化为热能) C.升高温度,该平衡正向速率减小,故平衡逆向移动 使用催化剂或缩小容器体积,该平衡均不会移动
2C(g)+D.(g) △H.=-a kJ/mol。5 min后达平衡,测得容器中n =0.8 mol。则下列说法正确的是( ) A.3vA.=2vC.=0.16 mol/(L·min) B.该可逆反应达平衡后,放出0.8a kJ的热能(假设化学能全转化为热能) C.升高温度,该平衡正向速率减小,故平衡逆向移动 使用催化剂或缩小容器体积,该平衡均不会移动
一定温度下,在密闭容器中进行的可逆反应 一定压力下的可逆反应 一定状态下的可逆反应 一定催化剂的可逆反应
可逆反应达到平衡时,正反应的平衡常数等于逆反应的平衡常数 可逆反应达到平衡时,正反应速率等于逆反应速率 可逆反应达到平衡时,参与反应的各物质的浓度保持不变 可逆反应达到平衡时,产物浓度幂的乘积与反应物浓度幂的乘积之比,在一定温度下是常数
不同的可逆反应,反应物的性质不同,平衡常数是相同的 对可逆反应来说,平衡常数越大,表示反应达到平衡时生成物浓度和反应物浓度的比值越大 对于同一个可逆反应,在不同温度下,平衡常数有相同的数值 对于可逆反应来说,平衡常数越大,也就是反应完成的程度越小,物质的转化率越大
改变反应条件可以改变该反应的限度 增大压强,正逆反应速率都增大 达到平衡时,SO2、O2、SO3在容器中共存 达到平衡时,SO2与SO3的浓度相等
正反应的速率与逆反应的速率相同程度增加 只增加正反应的速率 只增加逆反应速率 正反应速率比逆速率增加得快
不同的可逆反应,反应物的性质不同,平衡常数是相同的 对可逆反应来说,平衡常数越大,表示反应达到平衡时生成物浓度和反应物浓度的比值越大 对于同一个可逆反应,在不同温度下,平衡常数有相同的数值 对可逆反应来说,平衡常数越大,也就是反应完成的程度越小,物质的转化率越大
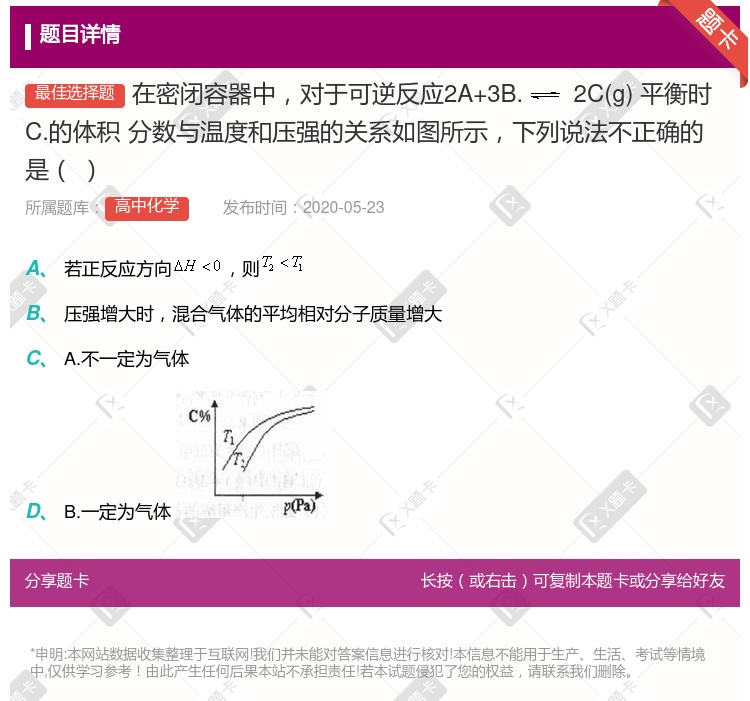
 2C(g)达到平衡时,测得A., , 物质的量之比为2:2:1。若保持温度不变,以2:2:1的物质的量之比再充入A.B.C.,下列判断正确的是( ) A.平衡向逆反应方向移动B.平衡不会发生移动 C.C的质量分数增大 C的质量分数减小
2C(g)达到平衡时,测得A., , 物质的量之比为2:2:1。若保持温度不变,以2:2:1的物质的量之比再充入A.B.C.,下列判断正确的是( ) A.平衡向逆反应方向移动B.平衡不会发生移动 C.C的质量分数增大 C的质量分数减小
 2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
 2C(g),可以判断达到化学平衡状态的是( ) A. 体系压强不变 单位时间消耗n molA,同时生成2nmolC A.的转化率不变 容器内气体密度不变
2C(g),可以判断达到化学平衡状态的是( ) A. 体系压强不变 单位时间消耗n molA,同时生成2nmolC A.的转化率不变 容器内气体密度不变
 2C(g)+D.(g) △H.=-a kJ/mol。5 min后达平衡,测得容器中n =0.8 mol。则下列说法正确的是( ) A.3vA.=2vC.=0.16 mol/(L·min) B.该可逆反应达平衡后,放出0.8a kJ的热能(假设化学能全转化为热能) C.升高温度,该平衡正向速率减小,故平衡逆向移动 使用催化剂或缩小容器体积,该平衡均不会移动
2C(g)+D.(g) △H.=-a kJ/mol。5 min后达平衡,测得容器中n =0.8 mol。则下列说法正确的是( ) A.3vA.=2vC.=0.16 mol/(L·min) B.该可逆反应达平衡后,放出0.8a kJ的热能(假设化学能全转化为热能) C.升高温度,该平衡正向速率减小,故平衡逆向移动 使用催化剂或缩小容器体积,该平衡均不会移动