你可能感兴趣的试题
C.N.、O.三种元素第一电离能从大到小的顺序是O.>N.>C. 根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 Ni原子的核外电子排布式为1s22s22p63s23p63d84s2
元素的第一电离能越大,其金属性越强
元素的第一电离能越小,其金属性越强
金属单质跟酸反应的难易,只跟该金属元素的第一电离能有关
同周期元素,第一电离能随原子序数增大逐渐增大
甲的金属性比乙强 乙的化合价为+1价 丙一定为非金属元素 丁一定是金属元素
的各级电离能数据如下: 则元素A.的常见价态是( ) A.+1 +2 +3 +6
第3周期所含的元素中钠的第一电离能最小 铝的第一电离能比镁的第一电离能大 在所有元素中,氟的电离能最大 钾的第一电离能比镁的第一电离能大
第一电离能越小,元素金属越强 第一电离能越小,该元素原子的能量越高 第一电离能越大,该元素的非金属性强 第一电离能失去的电子,一定是最外层上的电子
第3周期所含元素中钠的第一电离能最小 铝的第一电离能比镁的第一电离能大 在所有的元素中,F.的第一电离能最大 钾的第一电离能比镁的第一电离能大
族 ③R.元素第一电离能大于同周期相邻元素 ④R.元素基态原子的电子排布式为1s22s2 A.①② ②③ ③④ ①④
+1、+2、+3、+1
+2、+1、+3、+1
+3、+2、+1、+1
+1、+1、+3、+2
第一电离能是原子失去核外第一个电子需要的能量
在元素周期表中,主族元素的第一电离能从左到右越来越大
可通过各级电离能的数值,判断元素可能的化合价
第一电离能越大的元素,其电负性越大
QCl2 RCl
SCl3 TCl 
硼(1s22s22p1) 铍(1s22s2)
氦(1s2) 氢(1s1)
Q和R S和T
T和U R和U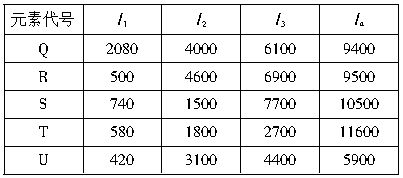
钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠 因同周期元素的原子半径从左到右逐渐减小,故第一电离能必定依次增大 最外层电子排布为ns2np6(若只有K.层时为1s2)的原子,第一电离能较大 对于同一元素而言,原子的逐级电离能越来越大
钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠 因同周期元素的原子半径从左到右逐渐减小,故第一电离能必依次增大 最外层电子排布为ns2np6(当只有K.层时为1s2)的原子,第一电离能较大 对于同一元素而言,原子的电离能I.123<…