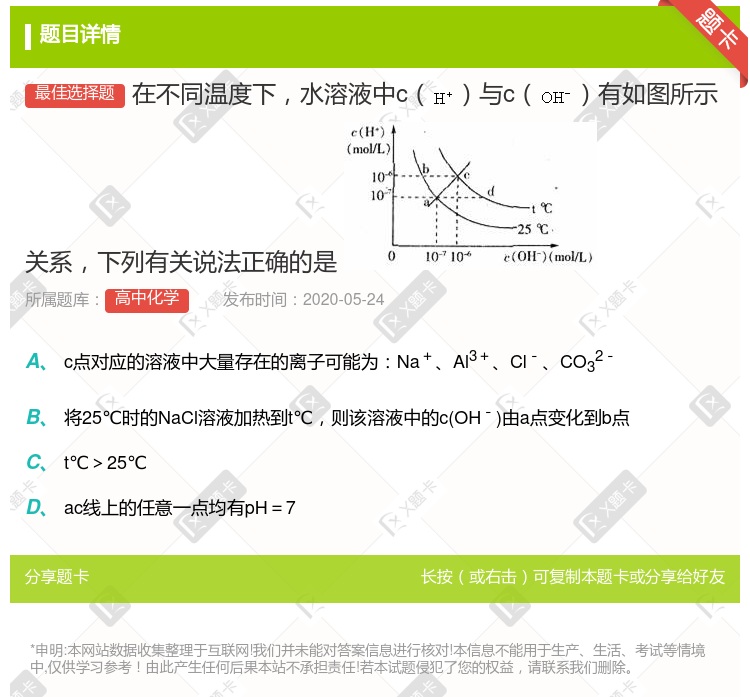

 b点对应的溶液中大量存在:NH
b点对应的溶液中大量存在:NH 、Ba2+、OH-、I.- c点对应的溶液中大量存在:Na+、Ba2+、Cl-、HCO
、Ba2+、OH-、I.- c点对应的溶液中大量存在:Na+、Ba2+、Cl-、HCO d点对应的溶液中大量存在:Na+、K.+、SO
d点对应的溶液中大量存在:Na+、K.+、SO 、Cl—
、Cl—
 b点对应的溶液中大量存在:NH
b点对应的溶液中大量存在:NH 、Ba2+、OH-、I.- c点对应的溶液中大量存在:Na+、Ba2+、Cl-、HCO
、Ba2+、OH-、I.- c点对应的溶液中大量存在:Na+、Ba2+、Cl-、HCO d点对应的溶液中大量存在:Na+、K.+、SO
d点对应的溶液中大量存在:Na+、K.+、SO 、Cl—
、Cl—

 、K.+、I.-、
、K.+、I.-、 c点对应的溶液中大量存在: Cu2+、Na+、Cl-、S2-
c点对应的溶液中大量存在: Cu2+、Na+、Cl-、S2-  d点对应的溶液中大量存在:K.+、AlO2-、ClO-、Cl-
d点对应的溶液中大量存在:K.+、AlO2-、ClO-、Cl-
 、K.+、I.-、
、K.+、I.-、 c点对应的溶液中大量存在: Cu2+、Na+、Cl-、S2- d点对应的溶液中大量存在:K.+、AlO2-、ClO-、Cl-
c点对应的溶液中大量存在: Cu2+、Na+、Cl-、S2- d点对应的溶液中大量存在:K.+、AlO2-、ClO-、Cl- 