你可能感兴趣的试题
三种酸的电离常数关系:KHM>KHN>KHR pH=7时,三种溶液中:c(M-)>c(N-)>c(R-) 当中和百分数达100%时,将三种溶液混合后:c(HM)+c(HN)+c(HR)=c(OH-)-c(H+) 滴定至P.点时,溶液中:c(HN)>c(N-)>c(Na+)>c(H+)>c(OH-)
B.C.三种物质的溶解度曲线,下列分析正确的是 ( ) 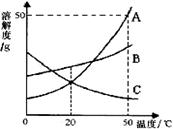 A.A.的溶解度比 大 B.50℃时把50gA放入100g水中能得到A.的饱和溶液,其中 溶质与溶液的质量比为1:2 将A.的饱和溶液变为不饱和溶液,可采用升温的方法 将50℃时A.B.C.三种物质的饱和溶液降温至20℃时, 这三种溶液的溶质质量分数的大小关系是B.>A.=C
A.A.的溶解度比 大 B.50℃时把50gA放入100g水中能得到A.的饱和溶液,其中 溶质与溶液的质量比为1:2 将A.的饱和溶液变为不饱和溶液,可采用升温的方法 将50℃时A.B.C.三种物质的饱和溶液降温至20℃时, 这三种溶液的溶质质量分数的大小关系是B.>A.=C
三种酸的电离常数关系:KHM>KHN>KHR pH=7时,三种溶液中:c(M-)>c(N-)>c(R-) 当中和百分数达100%时,将三种溶液混合后:c(HM)+c(HN)+c(HR)=c(OH-)-c(H+) 滴定至P.点时,溶液中:c(HN)>c(N-)>c(Na+)>c(H+)>c(OH-)
t2℃时,M.、N.、P.三种物质的溶解度由 大到小顺序是M.>N.>P. 将t2℃时的等质量三种物质的饱和溶液分 别降到0℃时,M.析出最多,P.无析出 若M.中含有少量N.,为了得到纯净的M., 可采用降温结晶的方法 若将t2℃三种物质的饱和溶液分别降到t1℃时,则三种溶液中溶质的质量分数由大到小的顺序是P.>N.>M.
三种酸的电离常数关系:KHM>KHN>KHR pH=7时,三种溶液中:c(M-)>c(N-)>c(R-) 当中和百分数达100%时,将三种溶液混合后:c(HM)+c(HN)+c(HR)=c(OH-)-c(H+) 滴定至P.点时,溶液中:c(HN)>c(N-)>c(Na+)>c(H+)>c(OH-)
t2 ℃时a、b、c三种物质的溶解度由大到小的顺序是 a>b>c t2 ℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水) 将t2 ℃时a、b、c三种物质的饱和溶液降温至t1 ℃时,所得溶液的溶质质量分数关系是b > a=c t1℃时a的饱和溶液的溶质质量分数为16.7%
B.C.三种物质的溶解度曲线,下列分析正确的是 A. 20℃时,三种物质的溶解度由大到小的顺序是B>A.>C 50℃时,A.的饱和溶液的溶质质量分数是50% 将50℃时100gA.B.C.三种物质的饱和溶液降温到20℃,析出固体A.最多 将20℃时三种物质的饱和溶液升高到50℃时,得到的都是 饱和溶液 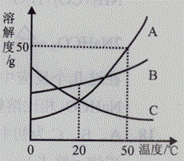
HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是 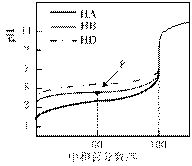 A.三种酸的电离常数关系:KHA>KHB>KHD 滴定至P.点时溶液中: c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) 当中和百分数达100%时,将三种溶液混合后: c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
A.三种酸的电离常数关系:KHA>KHB>KHD 滴定至P.点时溶液中: c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) 当中和百分数达100%时,将三种溶液混合后: c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
t2 ℃时a、b、c三种物质的溶解度由大到小的顺序是 a>b>c t2 ℃时,将50g a物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水) 将t2 ℃时a、b、c三种物质的饱和溶液降温至t1 ℃时,所得溶液的溶质质量分数关系是b > a=c t1℃时a的饱和溶液的溶质质量分数为16.7%
1 kW、100kW,2000 kW 1 kW、8 kW、20 kW 100 kW、800 kW、2 000 kW 10 kW、80 kW、200 kW
HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是( ) A.三种酸的电离常数关系:KHA>KHB>KHD 滴定至P.点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
HB和HD)溶液,滴定的曲线如图所示,下列判断错误的是 A.三种酸的电离常数关系:K.HA>K.HB>K.HD 滴定至P.点时,溶液中: c(B-)>c %(Na+)>c(HB)>c(H+)>c(OH-) pH=7时,三种溶液中:c(Ah-)=c(B-)=c(D-) 当中和百分数达100%时,将三种溶液混合后: c(HA)+c(HB)+c(HD)=ch_(OH-)-c(Hh+)
HB和HD)溶液,滴定曲线如图所示,下列判断错误的是( ) 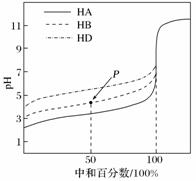 A.三种酸的电离常数关系:K.HA>K.HB>K.HD 滴定至P.点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) 当中和百分数达100%时,将三种溶液混合后: c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
A.三种酸的电离常数关系:K.HA>K.HB>K.HD 滴定至P.点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) 当中和百分数达100%时,将三种溶液混合后: c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)

 A.A.的溶解度比 大 B.50℃时把50gA放入100g水中能得到A.的饱和溶液,其中 溶质与溶液的质量比为1:2 将A.的饱和溶液变为不饱和溶液,可采用升温的方法 将50℃时A.B.C.三种物质的饱和溶液降温至20℃时, 这三种溶液的溶质质量分数的大小关系是B.>A.=C
A.A.的溶解度比 大 B.50℃时把50gA放入100g水中能得到A.的饱和溶液,其中 溶质与溶液的质量比为1:2 将A.的饱和溶液变为不饱和溶液,可采用升温的方法 将50℃时A.B.C.三种物质的饱和溶液降温至20℃时, 这三种溶液的溶质质量分数的大小关系是B.>A.=C

 A.三种酸的电离常数关系:KHA>KHB>KHD 滴定至P.点时溶液中: c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) 当中和百分数达100%时,将三种溶液混合后: c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
A.三种酸的电离常数关系:KHA>KHB>KHD 滴定至P.点时溶液中: c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) 当中和百分数达100%时,将三种溶液混合后: c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
 A.三种酸的电离常数关系:K.HA>K.HB>K.HD 滴定至P.点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) 当中和百分数达100%时,将三种溶液混合后: c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)
A.三种酸的电离常数关系:K.HA>K.HB>K.HD 滴定至P.点时,溶液中:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) 当中和百分数达100%时,将三种溶液混合后: c(HA)+c(HB)+c(HD)=c(OH-)-c(H+)