你可能感兴趣的试题
甲、乙两烧杯中溶液的pH均保持不变 甲烧杯中a的电极反应式为 ↑+2H2O 当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 当b极增重
↑+2H2O 当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 当b极增重 时,d极产生的气体为
时,d极产生的气体为 (标况)
(标况) 
铜是电解池的阳极 石墨电极附近溶液呈红色 铜电极上产生的是无色气体 石墨电极上发生还原反应 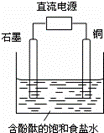
甲、乙两烧杯中溶液的pH均保持不变 乙烧杯中d的电极反应为2Cl- Cl2↑+2e- 乙烧杯中通入适量HCl气体,溶液组成可以恢复 a极产生11.2L(标准状况)气体时,c极产生2g气体
Cl2↑+2e- 乙烧杯中通入适量HCl气体,溶液组成可以恢复 a极产生11.2L(标准状况)气体时,c极产生2g气体
甲、乙两烧杯中溶液的pH均升高 当b极增重5.4g时,d极产生的气体为2.24L(标准状况) 当电解一段时间后,将甲、乙两溶液混合,一定会生成沉淀 乙烧杯中c的电极反应式为2Cl--2e-=Cl2↑
甲、乙两烧杯中溶液的pH均保持不变 甲烧杯中a的电极反应式为 4OH――4e-=O2↑+2H2O 当电解一段时间后,将甲、乙两溶液混合, 一定会产生蓝色沉淀 当b极增重3.2g时,d极产生的气体为2.24L(标况)
乙池中d的电极反应为2Cl--2e-=Cl2↑ a、c两极产生气体的物质的量相等 甲、乙两池中溶液的pH均保持不变 乙池中发生的反应为2NaCl+2H2O通电2NaOH+H2↑+Cl2↑
Mg 电极是该电池的正极 H2O2 在石墨电极上发生氧化反应 石墨电极附近溶液的pH 增大 溶液中Cl— 向正极移动
乙烧杯中的d电极反应式为Fe-2e-=Fe2+ 电解一段时间后,将甲、乙两溶液混合,一定会产生沉淀 当b极增重5.4g时,d极产生的气体为2.24L(标况) 甲烧杯中溶液的pH降低
铜电极附近观察到黄绿色气体 石墨电极附近溶液呈红色 溶液中的Na+向石墨电极移动  铜电极上发生还原反应
铜电极上发生还原反应
铜电极附近观察到黄绿色气体 石墨电极附近溶液呈红色  溶液中的Na+向石墨电极移动 铜电极上发生还原反应
溶液中的Na+向石墨电极移动 铜电极上发生还原反应
石墨电极是该电池的正极 石墨电极上发生还原反应 Mg电极的电极反应式:Mg-2e-=Mg2+ 电池工作时,电子从Mg电极经导线流向石墨电极,再从石墨电极经电解质溶液流向Mg电极
甲、乙两烧杯中溶液的pH均保持不变 乙烧杯中d的电极反应为2Cl―-2e―=Cl2↑ 乙烧杯中通入适量HCl气体溶液组成可以恢复 a极产生1.12L(标况)气体时,c极产生2g气体
石墨电极是该电池的正极 石墨电极上发生还原反应 Mg电极的电极反应式:Mg-2e-=Mg2+ 电池工作时,电子从Mg电极经导线流向石墨电极,再出石墨电极经电解质溶液流向Mg电极
同温、同压下,装置Ⅰ中石墨电极上方得到的气体比铁电极上方得到的气体多 用装置Ⅱ进行实验时铁电极的电极反应为Fe-2e-+2OH-===Fe(OH)2 用装置Ⅱ进行实验时石墨电极的电极反应为2H++2e-===H2↑ 装置Ⅰ通电10分钟后铁电极周围溶液pH降低
甲、乙两烧杯中溶液的pH均保持不变; 甲烧杯a电极反应式为:4OH― - 4e- = O2↑+ 2H2O 电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 当b极增重3.2g时,d极产生的气体为2.24L(标准状况下)

 ↑+2H2O 当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 当b极增重
↑+2H2O 当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 当b极增重 时,d极产生的气体为
时,d极产生的气体为 (标况)
(标况) 

 Cl2↑+2e- 乙烧杯中通入适量HCl气体,溶液组成可以恢复 a极产生11.2L(标准状况)气体时,c极产生2g气体
Cl2↑+2e- 乙烧杯中通入适量HCl气体,溶液组成可以恢复 a极产生11.2L(标准状况)气体时,c极产生2g气体

 铜电极上发生还原反应
铜电极上发生还原反应
 溶液中的Na+向石墨电极移动 铜电极上发生还原反应
溶液中的Na+向石墨电极移动 铜电极上发生还原反应