你可能感兴趣的试题
1是可逆反应; 2是可逆反应; 3是可逆反应; 1,2,3均不是可逆反应。
可逆反应,体积增大的放热反应 可逆反应,体积减小的吸热反应 可逆反应,体积增大的吸热反应
吸热可逆反应 吸热不可逆反应 放热不可逆反应 放热可逆反应
可逆反应达到平衡的重要特征是各物质的反应速率相等。 在可逆反应里,正反应的速率是正值,逆反应的速率是负值。 对于H2+I2  2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,叫做可逆反应。 所有的化学反应都是可逆的 有气体参加的反应或有气体生成的反应,一定要在密闭体系的条件下才能是可逆反应 可逆反应中,正反应和逆反应是相对的
放热反应和可逆反应 吸热反应和可逆反应 吸热反应和不可逆反应 放热反应和不可逆反应
同一条件下,化学反应既能向由反应物变成生成物的方向进行,又能向由生成物变成反应物的方向进行,这样的反应叫可逆反应 在化学反应中,大量的是不可逆反应,可逆反应只是少数 有的化学反应几乎只是向一个方向进行,这类反应称不可逆反应 因反应可同时向两个方向进行,可逆反应不能进行到底
在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,叫可逆反应 所有的化学反应都是可逆的 有气体参加的反应或有气体生成的反应,一定要在密闭体系的条件下才能是可逆反应 可逆反应中,正反应和逆反应是相对的
不同的可逆反应,反应物的性质不同,平衡常数是相等的 对可逆反应来说,平衡常数越大,表示反应达到平衡时生成物浓度和反应物浓度的比值越大 对于同一个可逆反应,在不同的温度下,平衡常数有相同的数值 对可逆反应来说,平衡常数越大,表示反应完成的程度越小,物质的转化率越大
可逆反应 总反应为不可逆反应 H2S净化度较胺法差 碱液吸收H2S的反应为不可逆反应
SO2+Br2+2H2O===H2SO4+2HBr与2HBr+H2SO4(浓) Br2+SO2↑+2H2O互为可逆反应 既能向正反应方向进行,又能向逆反应方向进行的反应叫做可逆反应 在同一条件下,同时向正、逆两个方向进行的反应叫做可逆反应 电解水生成氢气和氧气与氢气和氧气点燃生成水的反应是可逆反应
Br2+SO2↑+2H2O互为可逆反应 既能向正反应方向进行,又能向逆反应方向进行的反应叫做可逆反应 在同一条件下,同时向正、逆两个方向进行的反应叫做可逆反应 电解水生成氢气和氧气与氢气和氧气点燃生成水的反应是可逆反应
可逆反应正反应速率大于逆反应速率 可逆反应正反应速率小于逆反应速率 可逆反应正反应速率等于逆反应速率 逆反应速率为 0
一定温度下,在密闭容器中进行的可逆反应 一定压力下的可逆反应 一定状态下的可逆反应 一定催化剂的可逆反应
可逆反应达到平衡时,正反应的平衡常数等于逆反应的平衡常数 可逆反应达到平衡时,正反应速率等于逆反应速率 可逆反应达到平衡时,参与反应的各物质的浓度保持不变 可逆反应达到平衡时,产物浓度幂的乘积与反应物浓度幂的乘积之比,在一定温度下是常数
不同的可逆反应,反应物的性质不同,平衡常数是相同的 对可逆反应来说,平衡常数越大,表示反应达到平衡时生成物浓度和反应物浓度的比值越大 对于同一个可逆反应,在不同温度下,平衡常数有相同的数值 对于可逆反应来说,平衡常数越大,也就是反应完成的程度越小,物质的转化率越大
1是可逆反应 2是可逆反应 3是可逆反应 1、2、3均不是可逆反应
1是可逆反应 2是可逆反应 3是可逆反应 1、2、3均不是可逆反应
正反应的速率与逆反应的速率相同程度增加 只增加正反应的速率 只增加逆反应速率 正反应速率比逆速率增加得快
(g)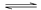 (g)+C(g),增大压强,正反应速率减小,逆反应速率增大 ⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大 A. 2 个 B. 3 个 4 个 5个
(g)+C(g),增大压强,正反应速率减小,逆反应速率增大 ⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大 A. 2 个 B. 3 个 4 个 5个
不同的可逆反应,反应物的性质不同,平衡常数是相同的 对可逆反应来说,平衡常数越大,表示反应达到平衡时生成物浓度和反应物浓度的比值越大 对于同一个可逆反应,在不同温度下,平衡常数有相同的数值 对可逆反应来说,平衡常数越大,也就是反应完成的程度越小,物质的转化率越大

 2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
 Br2+SO2↑+2H2O互为可逆反应 既能向正反应方向进行,又能向逆反应方向进行的反应叫做可逆反应 在同一条件下,同时向正、逆两个方向进行的反应叫做可逆反应 电解水生成氢气和氧气与氢气和氧气点燃生成水的反应是可逆反应
Br2+SO2↑+2H2O互为可逆反应 既能向正反应方向进行,又能向逆反应方向进行的反应叫做可逆反应 在同一条件下,同时向正、逆两个方向进行的反应叫做可逆反应 电解水生成氢气和氧气与氢气和氧气点燃生成水的反应是可逆反应
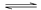 (g)+C(g),增大压强,正反应速率减小,逆反应速率增大 ⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大 A. 2 个 B. 3 个 4 个 5个
(g)+C(g),增大压强,正反应速率减小,逆反应速率增大 ⑦对达到平衡的一个放热的可逆反应,若降温,则正反应速率减小,逆反应速率增大 A. 2 个 B. 3 个 4 个 5个