你可能感兴趣的试题
原子序数=核电荷数 周期序数=电子层数 主族序数=最外层电子数 族元素最外层电子数为8
X.和R.在同一周期
原子半径:W.>R.>X
气态氢化物的稳定性:Y.>X
X.、Z.形成的化合物中只有离子键
元素原子最外层电子数是次外层电子数的2倍; 元素原子最外层电子数是其内层电子总数的3倍; 元素原子M.层电子数等于其L.层电子数的一半; 元素原子最外层有1个电子,D.的阳离子与B.的阴离子电子层结构相同,则4种元素原子序数关系中正确的是 A.C.>D.>B.>AB.D.>B.>A.>CC.A.>D.>C.>BD.B.>A.>C.>D
C>D.> >A B.D>B.>A.>C
A> >C.>B D.B>A.>C.>D
该图体现出原子核外电子层呈现周期性变化 简单离子半径:W.->R2->X+>S3+ R.、Z.形成的化合物中可能含有共价键 由酸性: HWO4>H2RO3可证明非金属性:W>R
该图体现出原子核外电子层呈现周期性变化 简单离子半径:W.->R2->X+>S3+ R.、Z.形成的化合物中可能含有共价键 由酸性: HWO4>H2RO3可证明非金属性:W>R
该图体现出原子核外电子层呈现周期性变化 原子半径:W>R>X X.、Z.形成的化合物中可能含有共价键 W.的氢化物与R.的氢化物水溶液的酸性比较,前者强于后者,可证明非金属性:R>W
X.与W.形成的化合物中只有共价键 X.与Z.形成的化合物中只有离子键 元素的非金属性:X.>R.>W. 简单离子的半径:W.>R.>X.
X.和R.在同一周期 原子半径:W.>R.>X. 气态氢化物的酸性:X.>Y. X.、Z.形成的化合物中阴阳离子个数比为1: 2
ZY、ZW、W2X的水溶液都显酸性 原子半径大小:W.>R.>X., 简单离子半径大小:R >W >X W.的氢化物与R.的氢化物水溶液的酸性比较,前者强于后者,可证明非金属性:R>W Z.与X.,Z.与R.两种元素形成的化合物中均可能存在共价键 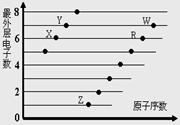
该图体现出原子核外电子层呈现周期性变化 原子半径:W>R>X X.、Z.形成的化合物中可能含有共价键 W.的氢化物与R.的氢化物水溶液的酸性比较,前者强于后者,可证明非金属性:R>W
X.与W.形成的化合物中只有共价键 X.与Z.形成的化合物中只有离子键 元素的非金属性:X.>R.>W. 简单离子的半径:W.>R.>X.
该图体现出原子核外电子层呈现周期性变化 原子半径:W>R>X X.、Z.形成的化合物中可能含有共价键 W.的氢化物与R.的氢化物水溶液的酸性比较,前者强于后者,可证明非金属性:R>W
X的最高价氧化物对应的水化物是弱酸 元素Z位于元素周期表的第3周期Ⅵ族 Y形成的单质能在二氧化碳中燃烧 原子半径的大小顺序: r(Z)>r(Y)>r(X)
X.和R.在同一周期
原子半径:W.>R.>X
气态氢化物的稳定性:Y.>X
X.、Z.形成的化合物中只有离子键
X.与W.形成的化合物中只有共价键 X.与Z.形成的化合物中只有离子键 元素的非金属性:X.>R.>W. 简单离子的半径:W.>R.>X.
元素非金属性:X.>R.>W. X.与R.形成的分子内含两种作用力 元素对应的离子半径:W.>R.>Y. X.、Z.形成的化合物中可能含有共价键

