你可能感兴趣的试题
石墨极上发生氧化反应 阳极的电极反应式为 除去
除去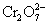 的反应:
的反应: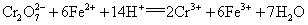 随着电解的进行,石墨极附近电解质溶液的pH会减小
随着电解的进行,石墨极附近电解质溶液的pH会减小
电极Y.应为Li 电解过程中,b中NaCl溶液的物质的量浓度将不断减小 X.极反应式为FeS+2Li++2e-===Fe+Li2S 若将图中阳离子膜去掉,将a、b两室合并,则电解反应总方程式发生改变
电极Y应为Li 电解过程中,b中NaCl溶液的物质的量浓度将不断减小 X极反应式为FeS+2Li++2e-===Fe+Li2S 若将图中阳离子膜去掉,将a、b两室合并,则电解反应总方程式发生改变
①②中Mg作负极,③④中Fe作负极 ②中Mg作正极,电极反应式为:6H2O+6e- == 6OH-+3H2↑ ③中Fe作负极,电极反应式为Fe-2e- == Fe2+ ④中Cu作正极,电极反应式为2H++2e- == H2↑
电极X.为Li 电解过程中,b中NaCl溶液的物质的量浓度将不断增大 X.极反应式为FeS+2Li++2e-=Fe+Li2S 若将图中阳离子膜去掉,将a、b两室合并,则电解反应总方程式发生改变 
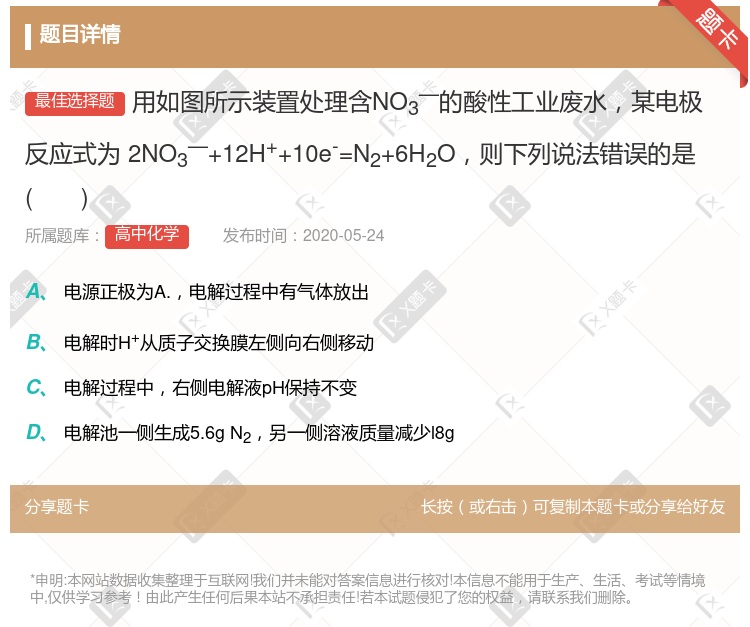
电源正极为A.,电解过程中有气体放出 电解时H+从质子交换膜左侧向右侧移动 电解过程中,右侧电解液pH保持不变 电解池一侧生成5.6g N2,另一侧溶液质量减少l8g
电源正极为A.,电解过程中有气体放出 电解时H+从质子交换膜左侧向右侧移动 电解过程中,右侧电解液pH保持不变 电解池一侧生成5.6g N2,另一侧溶液质量减少l8g
电极Y应为Li 电解过程中,b中NaCl溶液的物质的量浓度将不断减小 X极反应式为FeS+2Li++2e-===Fe+Li2S 若将图中阳离子膜去掉,将a、b两室合并,则电解反应总方程式发生改变
用石墨作阴极,铁作阳极 阴极的电极反应式为:2H2O + 2e- = H2↑ + 2OH- 阳极的电极反应式为:Cl- + 2OH--2e-= ClO- + H2O 除去CN-的反应:2CN-+5ClO-+ H2O =N2↑+2CO2↑+5Cl-+2OH-
 除去
除去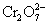 的反应:
的反应: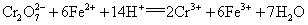 随着电解的进行,石墨极附近电解质溶液的pH会减小
随着电解的进行,石墨极附近电解质溶液的pH会减小
