你可能感兴趣的试题
pH = 0的NaHSO4溶液 0.04 mol·L-1 硫酸 0.5 mol·L-1 盐酸 0.05 mol·L-1硝酸
0.01 mol•L-1 0.017 mol•L-1 0.05 mol•L-1 0.50 mol•L-1
NaOH溶液与三种酸的反应均是吸热反应 酸性强弱: HX>HY>HZ 滴定酸HY可用酚酞作指示剂 滴定三种酸都可用甲基橙作指示剂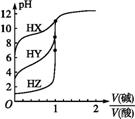
中和10 mL 0.1 mol·L-1 醋酸与中和100 mL 0.01 mol·L-1的醋酸所需同种碱溶液的量不同 常温下,等体积的pH=3的酸溶液和pH=11的碱溶液混合,混合后溶液的pH=7 常温下,体积相等、pH相同的盐酸和硫酸溶液,两溶液溶质的物质的量浓度相等 常温下,pH=3的甲酸溶液的c(H+)与pH=11的氨水溶液的c(OH-)相等
常温下,测得醋酸钠溶液的pH>7 常温下,测得0.1mol/L醋酸溶液的pH=4 常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4 常温下,将物质的量浓度相同的醋酸溶液与氢氧化钠溶液等体积混合后恰好中和
pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5mol/L pH=12的氨水加水稀释后溶液中所有离子浓度都减小 pH=2的HCl溶液与pH=13的NaOH溶液按体积比1:10混合后溶液呈中性 c(Na+)相同的①CH3COONa②NaHCO3③NaClO三种溶液的pH大小:③>②>①
相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等 常温下,测得0.1 mol·L-1醋酸溶液的pH=4 常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4 在相同条件下,醋酸溶液的导电性比盐酸的弱
常温下,pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 常温下,将pH =10的氨水稀释后,溶液中所有离子浓度都减小 常温下,0.1 mol/L Na2S溶液中存在:c(OH-) = c(H+) + c(HS-) + c(H2S) 常温下,pH为1的0.1 mol/L HA溶液与0.1 mol/L NaOH溶液恰好完全反应时,溶液中一定存在: c (Na+) = c(A-) > c(OH-) = c(H+)
常温下同浓度的强酸、强碱等体积混合后由水电离出的c(H+) =10-7mol·L-l 常温下pH =2的盐酸和pH =12的氨水等体积混合后c(C1-)+c(H+)=c(NH4+)+c(OH-) 常温下0.1 mol.L.-1的Na2A溶液的pH=10,则该溶液中由水电离的c(OH-)= 10 -10 mol.L.-l 常温下向10 mL0.1 mol.L.-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中, 将减小
将减小
常温下,测得醋酸钠溶液的pH>7
常温下,测得0.1 mol/L醋酸溶液的pH=4
常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4
常温下,将物质的量浓度相同的醋酸溶液与氢氧化钠溶液等体积混合后恰好中和
氨水溶液会使紫色石蕊溶液变红 常温下PH等于13的氨水溶液与PH等于1的盐酸溶液等体积混合后溶液的PH>7 常温下10ml的0.01mol/L氨水溶液测得PH值约为10 相同温度下,氨水导电能力比相同浓度氢氧化钠溶液的导电能力弱
常温下,pH等于14与pH等于12的两种NaOH溶液等体积混合后, c(H+)=(10-14+10-10)/2 常温下,浓度为1×10-10 mol·L.-1的KOH溶液的pH为7 氨水加水稀释,溶液中除水以外的所有粒子的浓度都减小 常温下,pH等于1的盐酸溶液中水的电离程度与pH等于13的Ba(OH)2溶液中水的电离程度相等
1∶10∶100∶1000 0∶1∶12∶11 14∶13∶12∶11 14∶13∶2∶3


 将减小
将减小