你可能感兴趣的试题
1s22s12p2 1s22s22p33s1 1s22s22p63s14s1 1s22s22p63s23p64s1
第一电离能:④>③>②>① 原子半径:④>③>②>① 电负性:④>③>②>① 最高正化合价④>③=②>①
C.  P.原子价电子轨道表示式
P.原子价电子轨道表示式 Cr原子的价电子排布式 3d44s2 Fe2+ 1s22s22p63s23p63d64s2
Cr原子的价电子排布式 3d44s2 Fe2+ 1s22s22p63s23p63d64s2
1s22s1 1s22s22p5 1s22s22p63s2 1s22s22p63s23p64s1
ls22s22p63s23p5 1s22s22p3 1s22s22p2 1s22s22p63s23p2
第一电离能:③>②>① 原子半径:③>②>① 电负性:③>②>① 最高正化合价:③>②>①
同一原子中,2p、3p、4p能级的轨道数依次增多 电子排布式(22Ti)1s22s22p63s23p10违反了能量最低原则 共价键都有方向性 正三价阳离子的电子排布式为1s22s22p63s23p63d5的元素在周期表中位于Ⅷ族
1s22s22p63s23p1 1s22s22p5 1s22s22p63s23p4 1s22s22p1
Na+的轨道表示式: Na+的结构示意图:
Na+的结构示意图: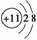 Na的电子排布式:1s22s22p63s1 Na的简化电子排布式:[Ne]3s1
Na的电子排布式:1s22s22p63s1 Na的简化电子排布式:[Ne]3s1
Na+:1s22s22p6 F:1s22s22p5 O2—:1s22s22p4 Ar:1s22s22p63s23p6
C. 1s22s22p2 O2- 1s22s22p6 Cr 1s22s22p63s23p63d44s2 Al3+ 1s22s22p6
具有下列电子排布式的原子中,①1s22s22p63s23p2②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4 原子半径最大的是① 具有下列价电子排布式的原子中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4,第一电离能最 大的是③ ①Na、K.、Rb ②O.、S.、Se ③Na、P.、Cl,元素的电负性随原子序数增大而递增的是③ 某元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703, 当它与氯气反应时可能生成的阳离子是X3+
具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s222s2p63s23p4 原子半径最大的是① 具有下列价电子排布式的原子中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4 第一电离能最大是③ ①Na、K.、Rb ②N.、P.、As ③O.、S.、Se ④Na、P.、Cl,元素的电负性随原子序数增大而递增的是④ 某元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X3+
最高正化合价:③>②>① 原子半径:③>②>① 电负性:③>②>① 第一电离能:③>②>①
1s22s22p5 1s22s22p43s2 1s22s22p63s23p63d54s1 1s22s22p63s23p63d34s2

 P.原子价电子轨道表示式
P.原子价电子轨道表示式 Cr原子的价电子排布式 3d44s2 Fe2+ 1s22s22p63s23p63d64s2
Cr原子的价电子排布式 3d44s2 Fe2+ 1s22s22p63s23p63d64s2
 Na+的结构示意图:
Na+的结构示意图: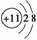 Na的电子排布式:1s22s22p63s1 Na的简化电子排布式:[Ne]3s1
Na的电子排布式:1s22s22p63s1 Na的简化电子排布式:[Ne]3s1