你可能感兴趣的试题
Fe(NO3)x中的x为2
稀HNO3在反应中只表现氧化性
磁性氧化铁中的所有铁元素全部被氧化
反应中每还原0.3mol氧化剂,就有0.9mol电子转移
如果硝酸的量不足,则应该有Fe(NO3)2生成 上述反应配平后HNO3的化学计量数为10 若有0.1mol HNO3被还原,则生成2.24L NO气体 23.2g磁性氧化铁完全溶解于稀硝酸中,转移0.1mol电子
Fe(NO3)x中的x为2 反应中每还原0.4 mol氧化剂,就有1.2 mol电子转移 稀硝酸在反应中只表现氧化性 磁性氧化铁中的所有铁元素全部被氧化
Fe(NO3)x中的x为2 反应中每还原0.4 mol氧化剂,就有1.2 mol电子转移 稀HNO3在反应中只表现氧化性 磁性氧化铁中的所有铁元素全部被氧化
Fe(NO3)X中的X.为2 稀HNO3在反应中只表现氧化性 反应中每还原0.4mol氧化剂,就有1.2mol电子转移 磁性氧化铁中的所有铁元素全部被氧化
Fe(NO3)x中的x为2 反应中每还原0.2 mol氧化剂,就有0.6 mol电子转移 稀HNO3在反应中只表现氧化性 磁性氧化铁中的所有铁元素全部被氧化
3 Cu + 8 HNO3(稀) ======= 3 Cu(NO3)2 + 2 NO↑+ 4 H2O CuO + 2 HNO3(稀) ======= Cu(NO3)2 + H2O C.+ 4 HNO3(浓) ======= CO2 ↑ + 4 NO2↑ +2 H2O 3 Ag + 4 HNO3(稀) ======= 3 AgNO3 + NO↑ +2 H2O
Fe (NO3)x中的x为2 反应中每生成0.2 mol 还原产物,就有0.6 mol 电子转移 稀HNO3 在反应中只作氧化剂 磁性氧化铁中的铁元素全部被氧化
Fe(NO3)x中的x为2 反应中每还原0.2 mol氧化剂,就有0.6 mol电子转移 稀HNO3在反应中只表现氧化性 磁性氧化铁中的所有铁元素全部被氧化
Ⅰ中气体有无色变红棕色的化学方程式为2NO+O2===2NO2 Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
Fe(NO3)x中的x为2 磁性氧化铁中的铁元素全部被氧化 纳米四氧化三铁可分散在水中,它与FeCl3溶液的分散质直径相当 反应中每生成0.4mol还原产物,就有1.2mol电子转移
中Fe(NO3)x的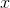 为2 反应中每生成0.1mol还原产物,就有0.6mol电子转移
为2 反应中每生成0.1mol还原产物,就有0.6mol电子转移
稀HNO3在反应中只作氧化剂 磁性氧化铁中的铁元素部分被氧化
Fe(NO3)x中的x为2 反应中每生成0.2 mol 还原产物,就有0.6 mol 电子转移 稀HNO3 在反应中只作氧化剂 磁性氧化铁中的铁元素全部被氧化
将铜屑加入Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+ 将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑ 将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
将铜屑加入Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+ 将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑ 将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
将铜屑加入Fe3+溶液中:2Fe3+ + Cu = 2Fe2+ + Cu2+ 将磁性氧化铁溶于盐酸:Fe3O4 + 8H+ = 3Fe3+ + 4H2O 将氯化亚铁溶液和稀硝酸混合:Fe2+ + 4H+ + NO3- =Fe3+ +2H2O + NO↑ 将铁粉加入稀硫酸中:2Fe + 6H+ + =2Fe3+ +3H2↑
Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2 → 2NO2 Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 针对III中现象,在Fe、Cu之间连接电流计,可判断Fe是否持续被氧化

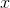 为2 反应中每生成0.1mol还原产物,就有0.6mol电子转移
为2 反应中每生成0.1mol还原产物,就有0.6mol电子转移