你可能感兴趣的试题
(Q1+Q2+Q3)kJ 0.5(Q1+Q2+Q3)kJ (0.5Q1-1.5Q2+0.5Q3)kJ (1.5Q1-0.5Q2+0.5Q3)kJ
放出的热量为(0.4Q1+0.1Q3)KJ 放出的热量为(0.4Q1+0.05Q2)KJ 放出的热量为(0.4Q1+0.05Q3)KJ △H2 <△H3
(Q1+Q2+Q3) kJ 0.5(Q+Q2+Q3) kJ (0.5Q1-1.5Q2+0.5Q3) kJ (3Q1-Q2+Q3) kJ
(Q.1+Q.2+Q.3) kJ [0.5(Q.1+Q.2+Q.3)] kJ (0.5Q.1-1.5Q.2+0.5Q.3) kJ (1.5Q.1-0.5Q.2+0.5Q.3) kJ
(Q.1+Q.2+Q.3) kJ 0.5(Q.1+Q.2+Q.3) kJ (0.5Q.1-1.5Q.2+0.5Q.3) kJ (3Q.1-Q.2+Q.3) kJ
(Q1+Q2+Q3) kJ 0.5(Q+Q2+Q3) kJ (0.5Q1-1.5Q2+0.5Q3) kJ (3Q1-Q2+Q3) kJ
放出的热量为(0.4Q1+0.05Q3)KJ/mol 放出的热量为(0.4Q1+0.05Q2)KJ/mol △H2 > △H3 △H2 <△H3
0.4Q1+0.1Q2 0.4Q1+0.05Q2 0.4Q1+0.1Q3 0.4Q1+0.05Q3
(Q.1+Q2+Q3)kJ 0.5(Q.1+Q2+Q3)kJ (1.5Q.1 —0.5Q.2+0.5Q.3)kJ (0.5Q.1 —1.5Q.2+0.5Q.3)kJ
Q1+Q2+Q3 0.5Q3-Q2+2Q1 0.5Q3+Q2-2Q1 0.5(Q1+Q2+Q3)
放出的热量为(0.4Q1+0.05Q3)KJ/mol 放出的热量为(0.4Q1+0.05Q2)KJ/mol △H2<△H3 △H2=△H3
(Q1+Q2+Q3) kJ [0.5(Q1+Q2+Q3)] kJ (0.5Q1-1.5Q2+0.5Q3) kJ (1.5Q1-0.5Q2+0.5Q3) kJ
2Q1>O2 Q1>2Q2 2Q1<Q2 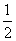 Q2=Q1
Q2=Q1
(Q1+Q2+Q3) kJ [0.5(Q1+Q2+Q3)] kJ (0.5Q1-1.5Q2+0.5Q3) kJ (1.5Q1-0.5Q2+0.5Q3) kJ
(Q.1+Q.2+Q.3) kJ [0.5(Q.1+Q.2+Q.3)] kJ (0.5Q.1-1.5Q.2+0.5Q.3) kJ (1.5Q.1-0.5Q.2+0.5Q.3) kJ
Q1 +Q2 +Q3 0.5(Q1 +Q2 +Q3) 0.5Q1 –0.5Q2 +0.5Q3 1.5Q1 –0.5Q2 +0.5Q 3
4Q1+0.5Q3 4Q1+0.5Q2 4Q1+Q3 4Q1+2Q2
(4Q.1+4Q.2+4Q.3)kJ (2Q.1-2Q.2+6Q.3 )kJ [2(Q.1+Q.2+Q.3)] kJ (2Q.1-6Q.2+2Q.3)kJ
Q.1=Q.2 Q.2> Q.1 Q.21 无法比较 C. 10.下列依据热化学方程式得出的结论正确的是 A.若2H2(g)+O2(g) =2H2O(g) ΔH=—483.6 kJ·mol-1,则H2燃烧热为241.8 kJ·mol-1 B.若C.(石墨,s) =C(金刚石,s) ΔH>0,则石墨比金刚石稳定 C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=—57.4 kJ·mol-1,则20.0g NaOH固体与稀盐酸完全中和,放出28.7 kJ的热量 D.已知2C(s)+2O2(g) =2CO2(g) ΔH1;2C(s)+O2(g) =2CO(g) ΔH2,则ΔH1>ΔH2

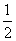 Q2=Q1
Q2=Q1