你可能感兴趣的试题
镁为负极 原电池中碳极的电极反应式为 电解池中阳极处先变红 电解池中阴极的电极反应式为
电解池中阳极处先变红 电解池中阴极的电极反应式为

电解过程中,铜电极上有H2产生 电解过程中,铜电极不断溶解 电解过程中,石墨电极上始终有铜析出 整个电解过程中,H.+的浓度不断增大
查看实验装置是否漏气 将红磷改为蜡烛再重做实验 实验中红磷的量可能不足,没有将瓶内氧气完全消耗 反应后未冷却至室温就打开止水夹,使进入瓶内水的体积减少
实验②③对照可以证明植物生具有向光性 实验③进行一段时间后,青菜叶片发黄的原因是无光条件叶绿素不能合成 实验④的生长结果只能证明根的生长具有向地性 实验①的目的是对实验②③④起对照作用
镁为负极 原电池碳极上反应为Fe3++e-―→Fe2+ 电解池中阳极处变红,阴极处变蓝 电解池阴极的反应为2H++2e-―→H2↑ 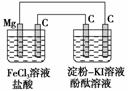
电解一段时间后,向Ⅱ装置通入适量的HCl气体可以恢复原来的浓度 反应初期,Y电极周围出现白色沉淀 B电极质量增加 X电极产生气泡,且生成1mol气体的同时,有1molA参与反应
输氧时,a导管连接供给氧气的钢瓶 输氧时,该装置也能用来观测氧气输出的速率 实验室中将该装置装满水收集氧气时,气体从a导管进入 实验室中将该装置盛浓硫酸干燥氧气时,气体从a导管进入
鸡蛋壳发生了分解反应 I.中发生的现象为鸡蛋壳逐渐溶解,产生大量气泡 Ⅱ中的澄清石灰水变浑浊 Ⅲ中紫色石蕊试液变红。但第Ⅲ步是多余的
电解过程中,铜电极上有H2产生 电解初期,主反应方程式为:Cu+H2SO4 CuSO4+H2↑ 电解一定时间后,石墨电极上有铜析出 整个电解过程中,H+的浓度不断减少
CuSO4+H2↑ 电解一定时间后,石墨电极上有铜析出 整个电解过程中,H+的浓度不断减少
电解过程中,铜极上有H2生成 电解初期,主反应方程式为:2H2O=H2↑+O2↑ 整个电解过程中,H+的浓度不断增大 电解一定时间后,石墨电极上有铜析出
电解过程中,铜电极上有H2产生 电解初期,主反应方程式为:Cu+H2SO4 CuSO4+H2↑ 电解一定时间后,石墨电极上有铜析出 整个电解过程中,H.+的浓度不断增大
CuSO4+H2↑ 电解一定时间后,石墨电极上有铜析出 整个电解过程中,H.+的浓度不断增大
不通空气时,冷水中的白磷不燃烧  通空气时,冷水中的白磷不燃烧 不通空气时,热水中的白磷不燃烧 通空气时,热水中的白磷不燃烧
通空气时,冷水中的白磷不燃烧 不通空气时,热水中的白磷不燃烧 通空气时,热水中的白磷不燃烧
鸡蛋壳发生了分解反应 Ⅰ中发生的现象为鸡蛋壳逐渐溶解,产生大量气泡 II中的澄清石灰水变浑浊 III中紫色石蕊试液变红
电解过程中,铜电极上有H2产生 电解初期,主反应方程式为:Cu+H2SO4 CuSO4+H2↑ 电解一定时间后,石墨电极上无铜析出 整个电解过程中,H.+的浓度不断增大
CuSO4+H2↑ 电解一定时间后,石墨电极上无铜析出 整个电解过程中,H.+的浓度不断增大
本实验能说明镁与稀盐酸反应时,有气体放出 本实验能说明与稀盐酸反应时,镁屑比镁条更快 本实验能说明镁与稀盐酸反应有热量放出 本实验能说明温度降低时,分子间间隔变小
红磷燃烧一停止立即打开弹簧夹 实验前一定要检验装置的气密性 此实验可以证明氧气约占空气体积的1/5 将红磷换成硫粉,瓶中的水换成浓氢氧化钠溶液进行实验,也能得出相同结论
两图都属于对产品的过程评价 两图都属于对产品的结果评价 甲图是对产品按一般原则进行的评价 乙图是对产品按设计要求进行的评价
电解过程中,铜电极上有H2产生 电解过程中,铜电极不断溶解 电解过程中,石墨电极上始终有铜析出 整个电解过程中,H.+的浓度不断增大

 电解池中阳极处先变红 电解池中阴极的电极反应式为
电解池中阳极处先变红 电解池中阴极的电极反应式为


 CuSO4+H2↑ 电解一定时间后,石墨电极上有铜析出 整个电解过程中,H+的浓度不断减少
CuSO4+H2↑ 电解一定时间后,石墨电极上有铜析出 整个电解过程中,H+的浓度不断减少
 CuSO4+H2↑ 电解一定时间后,石墨电极上有铜析出 整个电解过程中,H.+的浓度不断增大
CuSO4+H2↑ 电解一定时间后,石墨电极上有铜析出 整个电解过程中,H.+的浓度不断增大
 通空气时,冷水中的白磷不燃烧 不通空气时,热水中的白磷不燃烧 通空气时,热水中的白磷不燃烧
通空气时,冷水中的白磷不燃烧 不通空气时,热水中的白磷不燃烧 通空气时,热水中的白磷不燃烧
 CuSO4+H2↑ 电解一定时间后,石墨电极上无铜析出 整个电解过程中,H.+的浓度不断增大
CuSO4+H2↑ 电解一定时间后,石墨电极上无铜析出 整个电解过程中,H.+的浓度不断增大