你可能感兴趣的试题
a为直流电源的负极 阴极的电极反应式为: 2HSO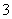 +2H++e-===S2O
+2H++e-===S2O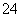 +2H2O 阳极的电极反应式为:SO2+2H2O-2e-===SO
+2H2O 阳极的电极反应式为:SO2+2H2O-2e-===SO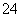 +4H+ 电解时,H.+由阴极室通过阳离子交换膜到阳极室
+4H+ 电解时,H.+由阴极室通过阳离子交换膜到阳极室
为直流电源,a、b都是惰性电极,通电 一段时间后,b极附近溶液呈红色。下列说法中正确的是  A.x是阳极,y是阴极 Pt电极的质量增加 a是正极,b是负极 CuCl2溶液的pH值基本不变,U.形管溶液pH值减小
A.x是阳极,y是阴极 Pt电极的质量增加 a是正极,b是负极 CuCl2溶液的pH值基本不变,U.形管溶液pH值减小
a为直流电源的负极 阴极的电极反应式为:2HSO3-+2H2O+2e-=S2O42-+2OH- 阳极的电极反应式为:SO2+2H2O-2e-=SO42-+4H+ 电解时,H.+由阴极室通过阳离子交换膜到阳极室
a为直流电源的负极 阴极的电极反应式为:2HSO3﹣+2H++e﹣═S2O.42﹣+2H2O. 阳极的电极反应式为:SO2+2H2O.﹣2e﹣═SO42﹣+4H+ 电解时,H.+由阴极室通过阳离子交换膜到阳极室
电极a连接的是电源的正极 若电路中转移0.03mole-,则离子交换膜左侧溶液中增加0.03mol离子 图中的离子交换膜是阳离子交换膜 阴极的电极反应式为2HSO3-+2e-+2H+==S2O42-+2H2O
a电极反应式为4OH--4e-===2H2O+O2↑ 产物丙为硫酸 d为阴离子交换膜 Na2SO4溶液浓度减小
马口铁(镀锡铁)镀层破损铁的腐蚀速率加快 为了防止钢铁设备腐蚀,利用外加电流的阴极保护法,应另附加一惰性电极,惰性电极作阴极 可以采用改变金属组成或结构的方法防止金属腐蚀 为保护海轮的船壳,利用牺牲阳极的阴极保护法,常在船壳上镶入锌块
a极与电源的负极相连 产物丙为硫酸溶液 离子交换膜d为阴离子交换膜 a电极反应式:2H2O+2e-=H2↑+2OH-
a电极反应式为2H++2e-===H2↑ 产物丙为硫酸 d为阴离子交换膜 Na2SO4溶液浓度增大
B.电极为电解池的阴极 B.极区吸收5mo1 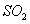 ,则A.极区生成2.5mo1
,则A.极区生成2.5mo1 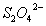 B.极区电解液为稀硫酸,电解一段时间后硫酸浓度增大 A.电极的电极反应为:
B.极区电解液为稀硫酸,电解一段时间后硫酸浓度增大 A.电极的电极反应为: 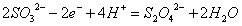
a极与电源的负极相连 产物丙为硫酸溶液 离子交换膜d为阴离子交换膜 a电极反应式:2H2O+2e-=H2↑+2OH-

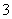 +2H++e-===S2O
+2H++e-===S2O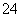 +2H2O 阳极的电极反应式为:SO2+2H2O-2e-===SO
+2H2O 阳极的电极反应式为:SO2+2H2O-2e-===SO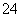 +4H+ 电解时,H.+由阴极室通过阳离子交换膜到阳极室
+4H+ 电解时,H.+由阴极室通过阳离子交换膜到阳极室
 A.x是阳极,y是阴极 Pt电极的质量增加 a是正极,b是负极 CuCl2溶液的pH值基本不变,U.形管溶液pH值减小
A.x是阳极,y是阴极 Pt电极的质量增加 a是正极,b是负极 CuCl2溶液的pH值基本不变,U.形管溶液pH值减小
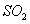 ,则A.极区生成2.5mo1
,则A.极区生成2.5mo1 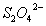 B.极区电解液为稀硫酸,电解一段时间后硫酸浓度增大 A.电极的电极反应为:
B.极区电解液为稀硫酸,电解一段时间后硫酸浓度增大 A.电极的电极反应为: