你可能感兴趣的试题
X.试剂可用Na2SO3饱和溶液 步骤Ⅲ的离子反应:2Br-+Cl2=2Cl-+Br2 工业上每获得1 mol Br2,需要消耗Cl2 44. 8L. 步骤IV包含萃取、分液和蒸馏
溴离子具有氧化性 氯气是还原剂 该反应属于复分解反应 氯气的氧化性比溴单质强
在浓海水中存在反应 Br2+H2O⇌HBr+HBrO 纯碱溶液显碱性的原因是 CO32﹣+2H2O⇌H2CO3+OH﹣ 海水中提取溴还可用到的反应 Cl2+2Br﹣═2Cl﹣+Br2 纯碱吸收溴的主要反应是3Br2+3Na2CO3═5NaBr+NaBrO3+3CO2↑
溴离子具有氧化性 氯气是还原剂 该反应属于复分解反应 氯气的氧化性比溴单质强
X.试剂可用Na2SO3饱和溶液 步骤Ⅲ的离子反应:2Br-+Cl2=2Cl-+Br2 工业上每获得1molBr2,需要消耗Cl244.8L 步骤Ⅳ包含萃取、分液和蒸馏
溴离子具有氧化性 氯气是还原剂 该反应属于复分解反应 氯气的氧化性比溴单质强
溴离子具有氧化性 氯气是还原剂
该反应属于复分解反应 氯气的氧化性比溴单质强
溴离子具有氧化性 氯气是还原剂 该反应属于复分解反应 氯气是氧化剂
用电子式表示溴化氢的形成过程为: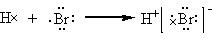 海水中Br-的电子式为:
海水中Br-的电子式为: 海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl 氯离子的结构示意图为:
海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl 氯离子的结构示意图为: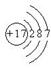
该反应属于置换反应 I-具有氧化性 1mol氯气转移了1mol电子 Cl2是还原剂
溴离子具有氧化性 溴单质是氧化剂 该反应属于复分解反应 氯元素的非金属性比溴元素弱
从海水中提取溴单质的过程一定涉及氧化还原反应 从海水中可以得到MgCl2,电解MgCl2溶液可制备Mg和Cl2 天然气、乙醇和水煤气分别属于化石能源、不可再生能源和二次能源 Cu、Al、Hg可以分别用热还原CuO、Al2O3、HgO的方法得到

 海水中Br-的电子式为:
海水中Br-的电子式为: 海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl 氯离子的结构示意图为:
海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl 氯离子的结构示意图为: