
 2NH3(g) ΔH=-38.6 kJ·mol-1 已知在120 ℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+1/2O2(g)===H2O(g) ΔH=-242 kJ·mol-1 25 ℃、101 kPa时,强酸与强碱的稀溶液发生反应的中和热为57.3 kJ·mol-1,硫酸稀溶液与氢氧化钾稀溶液反应的热化学方程式为:H2SO4(aq)+2KOH(aq)= K2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1 已知在120 ℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为H2(g)+1/2O2(g)===H2O(g) ΔH=-242 kJ·mol-1 25 ℃、101 kPa时,强酸与强碱的稀溶液发生反应的中和热为57.3 kJ·mol-1,硫酸稀溶液与氢氧化钾稀溶液反应的热化学方程式为:H2SO4(aq)+2KOH(aq)= K2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
 2NH3(g) △H1; CaCO3(s) == CaO(s)+CO2 (g) △H2 C.(s)+
2NH3(g) △H1; CaCO3(s) == CaO(s)+CO2 (g) △H2 C.(s)+ O2(g) == CO(g) △H1;C.(s)+O2(g) == CO2(g) △H2 H2(g)+Cl2(g) ==2HCl(g) △H1;
O2(g) == CO(g) △H1;C.(s)+O2(g) == CO2(g) △H2 H2(g)+Cl2(g) ==2HCl(g) △H1;  H2(g)+
H2(g)+ Cl2(g) == HCl(g) △H2
Cl2(g) == HCl(g) △H2
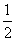 Cl2(g)===NaCl(s) ΔH1 Na(s)===Na(g) ΔH2 Na(g)-e-===Na+(g) ΔH3
Cl2(g)===NaCl(s) ΔH1 Na(s)===Na(g) ΔH2 Na(g)-e-===Na+(g) ΔH3
 O2(g)=SO3(g);ΔH.=-315 kJ·mol-1 表示中和热的热化学方程式NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l); ΔH.=-57.3 kJ·mol-1 表示H2燃烧热的热化学方程式H2(g)+
O2(g)=SO3(g);ΔH.=-315 kJ·mol-1 表示中和热的热化学方程式NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l); ΔH.=-57.3 kJ·mol-1 表示H2燃烧热的热化学方程式H2(g)+ O2(g)=H2O(g);ΔH.=-241.8 kJ·mol-1 表示CO燃烧热的热化学方程式2CO(g)+O2(g)=2CO2(g);ΔH.=-566 kJ·mol-1
O2(g)=H2O(g);ΔH.=-241.8 kJ·mol-1 表示CO燃烧热的热化学方程式2CO(g)+O2(g)=2CO2(g);ΔH.=-566 kJ·mol-1
 H2(g)+
H2(g)+ Cl2(g)===HCl(g) ΔH.=-91.5 kJ/mol
Cl2(g)===HCl(g) ΔH.=-91.5 kJ/mol