你可能感兴趣的试题
碳棒是正极 该装置能将电能转化为化学能 外电路中电流由铁片流出经过电流计流向碳棒 该装置的总反应为:2Fe+3Cu2+=2Fe3++3Cu
外电路中电流由铁片流出经过电流计流向碳棒 该装置能将电能转化为化学能 该装置的总反应为:2Fe+3Cu2+=2Fe3++3Cu 碳棒是正极
a为负极,是铁片,烧杯中的溶液为硫酸 b为负极,是铁片,烧杯中的溶液为硫酸铜溶液 a为正极,是碳棒,烧杯中的溶液为硫酸 b为正极,是碳棒,烧杯中的溶液为硫酸铜
外电路中电流由铁片流出经过电流计流向碳棒 该装置能将电能转化为化学能 该装置的总反应为:2Fe+3Cu2+=2Fe3++3Cu 碳棒是正极
a为负极,是铁片,烧杯中的溶液为硫酸G. 
 b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
b为负极,是铁片,烧杯中的溶液为硫酸铜溶液  a为正极,是碳棒,烧杯中的溶液为硫酸 b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
a为正极,是碳棒,烧杯中的溶液为硫酸 b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
a为负极,是铁片,烧杯中的溶液为硫酸
b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
a为正极,是碳棒,烧杯中的溶液为硫酸
b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
B.两根碳棒立在盛有硫酸铜的玻璃杯里。A.棒与电池正极相连, 棒与负极相连,如图所示,则下列叙述中正确的是 A. 溶液中电流是由铜原子从A.流向B.形成的 B. 溶液中的电流是由铜原子从B.流向A.形成的 几分钟后A.棒上将有一层红色的铜 几分钟后B.棒上将有一层红色的铜 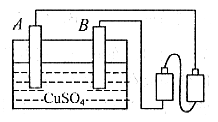
a为负极,是铁片,烧杯中的溶液为硫酸 b为负极,是铁片,烧杯中的溶液为硫酸铜溶液 a为正极,是碳棒,烧杯中的溶液为硫酸 b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
a为负极,是铁片,烧杯中的溶液为稀硫酸 b为负极,是铁片,烧杯中的溶液为硫酸铜溶液 a为正极,是碳棒,烧杯中的溶液为稀硫酸 b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
a为负极,是铁片,烧杯中的溶液为硫酸
b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
a为正极,是碳棒,烧杯中的溶液为硫酸
b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
若X.为铁棒,Y.为NaCl溶液, 开关K.置于M.处, 可减缓铁的腐蚀, 这种方法称为外接电源的阴极保护法 若整个装置为电解精炼铜的装置,则X.为粗铜,Y.为硫酸铜溶液,开关K.置于N.处,且电解过程中硫酸铜溶液浓度不变 若X.为碳棒,Y.为氯化铜溶液, 开关K.置于N.处, 当产生11.2L.气体时,右侧碳棒质量增加6. 4 g 若X.为碳棒,Y.为氯化钠溶液, 开关K.置于N.处, 当电路中有0.01 mol电子流过时,假设此时该溶液为100 mL,则常温下其pH为13
a为负极,是铁片,烧杯中的溶液为硫酸
b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
a为正极,是碳棒,烧杯中的溶液为硫酸
b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
a为负极,是铁片,烧杯中的溶液为硫酸
b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
a为正极,是碳棒,烧杯中的溶液为硫酸
b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
a为负极,烧杯中的溶液为稀硫酸 b为负极,烧杯中的溶液为硫酸铜溶液 a为正极,烧杯中的溶液为稀硫酸 b为正极,烧杯中的溶液为硫酸铜溶液 
X.是碳棒,Y.是金属铂,a是稀硫酸溶液,实质上是电解水,故溶液pH不变 X.是金属铂,Y.是碳棒,a是氯化钠溶液,在阴极上和阳极上析出气体的物质的量之比为1∶1 X.是金属铁,Y.是金属铜,a是硫酸铜溶液,X.极增重,溶液浓度减小 X.是精银,Y.是粗银,a是硝酸银溶液,在阴极上和阳极上析出产物的物质的量之比为1∶1
a为负极,是铁片,烧杯中的溶液为硫酸G. b为负极,是铁片,烧杯中的溶液为硫酸铜溶液 a为正极,是碳棒,烧杯中的溶液为硫酸 b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
a为负极,烧杯中的溶液为稀硫酸 b为负极,烧杯中的溶液为硫酸铜溶液 a为正极,烧杯中的溶液为稀硫酸 b为正极,烧杯中的溶液为硫酸铜溶液 
a为负极,是铁片,烧杯中的溶液为硫酸 b为负极,是铁片,烧杯中的溶液为硫酸铜溶液 a为正极,是碳棒,烧杯中的溶液为硫酸 b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液



 a为正极,是碳棒,烧杯中的溶液为硫酸 b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液
a为正极,是碳棒,烧杯中的溶液为硫酸 b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液


