你可能感兴趣的试题
62(a+b)g 186(a+b)g 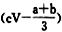 mol
mol 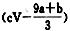 mol
mol
28.0 g 2.80 g 4.20 g 42.0 g
硝酸与金属反应时,主要是+5价的氮得电子 浓HNO3与浓HCl按3∶1的体积比所得的混合物叫王水 硝酸电离出的H.+离子,能被Zn、Fe等金属还原成H2 常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体
3.5 mol/L 4.5 mol/L 7.0 mol/L 9.0 mol/L
HNO3溶液 Ba(OH)2溶液 H2SO4溶液 HCl溶液
3.5mol·L-1 4.5mol·L -1 7.0mol·L -1 9.0mol·L -1
混合物中含有8gFeO
混合物中含有0.1molFeS
被还原的HNO3为1/3mol
参加反应的HNO3为1mol
HNO3溶液 Ba(OH)2溶液 H2SO4溶液 HCl溶液
HNO3 Ba(OH)2溶液 H2SO4溶液 HCl溶液
HNO3溶液 Ba(OH)2溶液 H2SO4溶液 HCl溶液
1 mol MnO2与含2 mol H2O2的溶液共热 1 mol铜投入含4 mol HNO3的浓硝酸中 1 mol铜与含2 mol H2SO4的浓硫酸共热 常温下1 mol铝片投入到足量浓硫酸中
HNO3中每个N.原子都得到4个电子 HNO3的还原产物可能为N.2O. HNO3的还原产物可能为HN4NO3 反应过程中HNO3共得到0.4摩电子
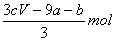 (a+3b)mol
(a+3b)mol 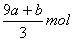 (cV-3a-9b)mol
(cV-3a-9b)mol
反应中有3a mol的电子转移 参加反应的HNO3为9a mol 氧化产物只有Fe(NO3)3 被还原的HNO3为3a mol
硝酸与金属反应时,主要是+5价的氮得电子 浓HNO3与浓HCl按3∶1的体积比所得的混合物叫王水 硝酸电离出的H.+离子,能被Zn、Fe等金属还原成H2 常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体
AgNO3 Fe2(SO4)3 稀HNO3 冷浓H2SO4

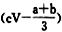 mol
mol 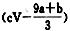 mol
mol
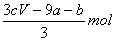 (a+3b)mol
(a+3b)mol 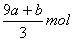 (cV-3a-9b)mol
(cV-3a-9b)mol