你可能感兴趣的试题
H2A在水溶液中的电离方程式为:H2A=H++HA-,HA- H++A2- 常温下,NH4HA溶液中滴加NaOH溶液至溶液pH=7,则c(Na+) = 2c(A2-) 相同条件下,体积相等、pH相等的盐酸与H2A溶液中和NaOH的量相等 0.0l mol·L-l的NaHA溶液pH>2
H++A2- 常温下,NH4HA溶液中滴加NaOH溶液至溶液pH=7,则c(Na+) = 2c(A2-) 相同条件下,体积相等、pH相等的盐酸与H2A溶液中和NaOH的量相等 0.0l mol·L-l的NaHA溶液pH>2
)>c(H+)。则下列说法(关系式)正确的是( )A.c (A2―) > c(H2A.) HA―的水解抑制了HA―的电离 HA―的水解和电离相互促进 c(OH―) = c(HA―)+c(A2―)+c(H2A.)
=H++HA-;HA- H++A2-。关于下列四种溶液的说法正确的是 ( ) ①0.01mol/L的H2A溶液;②0.01mol/L的NaHA溶液;③0.02mol/L的HCl溶液与0.04mol/L的NaHA溶液等体积混合;④0.02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合; A.四种溶液中c(HA-)浓度大小:③>②>①>④ 溶液①中一定不存在OH- 溶液②中存在水解平衡:HA-+H2O
H++A2-。关于下列四种溶液的说法正确的是 ( ) ①0.01mol/L的H2A溶液;②0.01mol/L的NaHA溶液;③0.02mol/L的HCl溶液与0.04mol/L的NaHA溶液等体积混合;④0.02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合; A.四种溶液中c(HA-)浓度大小:③>②>①>④ 溶液①中一定不存在OH- 溶液②中存在水解平衡:HA-+H2O H2A.+OH- 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
H2A.+OH- 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
====H++HA- HA- H.++A2- 在0.1mol·L-1Na2A溶液中存在的粒子,其浓度关系正确的是( ) A.c(Na+)+ c(H+)= c(O.H.-)+ c(HA-)+ c(A.2-) c(Na+)+ c(O.H.-)= c(H+)+ c(HA-) c(Na+)=2 c(A.2-)+2 c(HA-)+2 c(H.2A.) c(A.2-) + c(HA-)=0.1 mol·L-1
H.++A2- 在0.1mol·L-1Na2A溶液中存在的粒子,其浓度关系正确的是( ) A.c(Na+)+ c(H+)= c(O.H.-)+ c(HA-)+ c(A.2-) c(Na+)+ c(O.H.-)= c(H+)+ c(HA-) c(Na+)=2 c(A.2-)+2 c(HA-)+2 c(H.2A.) c(A.2-) + c(HA-)=0.1 mol·L-1
=H++HA-;HA- H++A2-。关于下列四种 溶液的说法正确的是 ( ) ①0.01mol/L的H2A溶液 ②0.01mol/L的NaHA溶液 ③0.02mol/L的HCl溶液与0.04mol/L的NaHA溶液等体积混合 ④0.02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合 A.四种溶液中c(HA-)浓度大小:③>①>②>④ 溶液①中一定不存在OH- 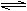 溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
pH=2的溶液中:c(H2A)+c(A2-)>c(HA-) E.点溶液中:c(Na+)-c(HA-)<0.100 mol·L.-1 c(Na+)=0.100 mol·L.-1的溶液中:c(H.+)+c(H2A)=c(OH-)+c(A2-) pH=7的溶液中:c(Na+)>2c(A2-)
0.01mol/L.的H2A溶液 0.01mol/L.的NaHA溶液 0.02mo|/L.的NaOH溶液与0.02 mol/L.的NaHA溶液等体积混合 0.02mol/L.的HCl溶液与0.04 mol/L.的NaHA溶液等体积混合
)最大的是( ) A.0.01 mol·L-1的H2A溶液 0.01 mol·L-1的NaHA溶液 0.02mol·L-1的HCl溶液与0.04mol·-1的NaHA溶液等体积混合 0.02mol·L-1的NaOH溶液与0.02mol·L-1的NaHA溶液等体积混合
c(Na+)=c(HA−)+2c(A.2−)+c(OH−) c(H.2A.)+c(HA−)+c(A.2−)=0.1 mol⋅L.−1
将上述溶液稀释至0.01mol/L.,c(H.+)⋅c(OH−) 不变 c(A.2−)+c(OH−)=c(H.+)+c(H.2A.)
=H++HA-;HA- H++A2-。关于下列四种 溶液的说法正确的是 ( ) ①0.01mol/L的H2A溶液 ②0.01mol/L的NaHA溶液 ③0.02mol/L的HCl溶液与0.04mol/L的NaHA溶液等体积混合 ④0.02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合 A.四种溶液中c(HA-)浓度大小:③>①>②>④ 溶液①中一定不存在OH-  溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
c(Na+)=c(HA-)+2c(A2-)+c(OH-) c(H2A.) + c(HA-) + c(A2-) = 0.1 mol・L-1 c(H+)・c(OH-)=10-14 c(A2-) + c(OH-) = c(H+) + c(H2A.)
=H++HA-;HA- H++A2-。关于下列四种 溶液的说法正确的是 ( ) ①0.01mol/L的H2A溶液 ②0.01mol/L的NaHA溶液 ③0.02mol/L的HCl溶液与0.04mol/L的NaHA溶液等体积混合 ④0.02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合 A.四种溶液中c(HA-)浓度大小:③>①>②>④ 溶液①中一定不存在OH-  溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)

 H++A2- 常温下,NH4HA溶液中滴加NaOH溶液至溶液pH=7,则c(Na+) = 2c(A2-) 相同条件下,体积相等、pH相等的盐酸与H2A溶液中和NaOH的量相等 0.0l mol·L-l的NaHA溶液pH>2
H++A2- 常温下,NH4HA溶液中滴加NaOH溶液至溶液pH=7,则c(Na+) = 2c(A2-) 相同条件下,体积相等、pH相等的盐酸与H2A溶液中和NaOH的量相等 0.0l mol·L-l的NaHA溶液pH>2
 H++A2-。关于下列四种溶液的说法正确的是 ( ) ①0.01mol/L的H2A溶液;②0.01mol/L的NaHA溶液;③0.02mol/L的HCl溶液与0.04mol/L的NaHA溶液等体积混合;④0.02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合; A.四种溶液中c(HA-)浓度大小:③>②>①>④ 溶液①中一定不存在OH- 溶液②中存在水解平衡:HA-+H2O
H++A2-。关于下列四种溶液的说法正确的是 ( ) ①0.01mol/L的H2A溶液;②0.01mol/L的NaHA溶液;③0.02mol/L的HCl溶液与0.04mol/L的NaHA溶液等体积混合;④0.02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合; A.四种溶液中c(HA-)浓度大小:③>②>①>④ 溶液①中一定不存在OH- 溶液②中存在水解平衡:HA-+H2O H2A.+OH- 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
H2A.+OH- 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
 H.++A2- 在0.1mol·L-1Na2A溶液中存在的粒子,其浓度关系正确的是( ) A.c(Na+)+ c(H+)= c(O.H.-)+ c(HA-)+ c(A.2-) c(Na+)+ c(O.H.-)= c(H+)+ c(HA-) c(Na+)=2 c(A.2-)+2 c(HA-)+2 c(H.2A.) c(A.2-) + c(HA-)=0.1 mol·L-1
H.++A2- 在0.1mol·L-1Na2A溶液中存在的粒子,其浓度关系正确的是( ) A.c(Na+)+ c(H+)= c(O.H.-)+ c(HA-)+ c(A.2-) c(Na+)+ c(O.H.-)= c(H+)+ c(HA-) c(Na+)=2 c(A.2-)+2 c(HA-)+2 c(H.2A.) c(A.2-) + c(HA-)=0.1 mol·L-1
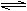 溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
 溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
 溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)
溶液②中存在水解平衡:HA—+H2O H2A.+OH— 溶液③中有关离子浓度关系:c(HA-)+c(A2-)=c(Na+)