
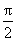 ,0)中心对称 B. 关于点(
,0)中心对称 B. 关于点( ,0)中心对称 关于点(0,0)中心对称
,0)中心对称 关于点(0,0)中心对称
 ) f′(x)=4sin(2x+
) f′(x)=4sin(2x+ ) f′(x)=sin(4x+
) f′(x)=sin(4x+ ) f′(x)=2sin(4x+
) f′(x)=2sin(4x+ )
)
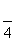 ) ( )y=2sin(2x+
) ( )y=2sin(2x+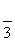 ) ( )y=2sin(2x–
) ( )y=2sin(2x–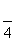 ) ( )y=2sin(2x–
) ( )y=2sin(2x–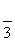 )
)
 ) y=2sin(2x+
) y=2sin(2x+ ) y=2sin(2x﹣
) y=2sin(2x﹣ ) y=2sin(2x﹣
) y=2sin(2x﹣ )
)
 ) g(x)=2sin(2x+
) g(x)=2sin(2x+ ) g(x)=2sin2x g(x)=2sin(2x﹣
) g(x)=2sin2x g(x)=2sin(2x﹣ )
)
 f(x)=2sin
f(x)=2sin f(x)=2sin
f(x)=2sin f(x)=2sin
f(x)=2sin