你可能感兴趣的试题
2、6、3、5 3、1、2、2 3、1、2、1 1、3、2、2
加入少量W.,逆反应速率增大 当容器中气体压强不变时,反应达到平衡 升高温度,平衡逆向移动 改变条件,又达新平衡,此时上述反应的平衡常数K.值一定增大
(g)+n (g)  p (g)+q (g),
p (g)+q (g), 若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图15所示,则对该反应的叙述正确的是( ) A.正反应是吸热反应B.逆反应是放热反应 C.m+np+q
若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图15所示,则对该反应的叙述正确的是( ) A.正反应是吸热反应B.逆反应是放热反应 C.m+np+q
加催化剂 向密闭容器中加入氩气 降低温度 增大反应物中NO的浓度 
(g)+ nB(g) pC(g)+ qD(g)在一密闭容器中进行,测得平均反应速度vC.= 2v 。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是( ) A.2、6、3、5B.3、1、2、2 3、1、2、1 1、3、2、2
pC(g)+ qD(g)在一密闭容器中进行,测得平均反应速度vC.= 2v 。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是( ) A.2、6、3、5B.3、1、2、2 3、1、2、1 1、3、2、2
2、1、2、1 3、1、2、2 2、6、3、5 1、3、2、2
P.、Q.、R.、S.的浓度相等 P.、Q.、R.、S.在容器中共存 P.、Q.、R.、S.的浓度不再变化 P.、Q.的消耗速率相等
①为30 g ②为20 g ③为22.5 g ④为77.5 g
CO全部转化为乙醇 断4NA个H-H键的同时,生成46g乙醇 若反应在恒温恒容密闭容器中进行,容器中混合气体的密度不再改变 若反应在绝热恒容密闭容器中进行,容器中温度不再改变
加催化剂 降低温度 增大反应物中NO的浓度 向密闭容器中加入氩气
P.、Q.、R.、S.的浓度相等 P.、Q.、R.、S.在密闭容器中共存 P.、Q.、R.、S.的浓度不再变化 用P.的浓度变化表示的化学速率与用Q.的浓度表示的化学反应速率相等
2、6、3、5 3、1、2、2 2、1、2、1 1、3、2、2
平衡前,随着反应的进行,容器内压强始终不变 平衡时,其它条件不变,分离出硫,正反应速率加快 平衡时,其它条件不变,升高温度可提高SO2的转化率 其它条件不变,使用不同催化剂,该反应的平衡常数不变
2、6、3、5 3、1、2、2 3、1、2、1 1、3、2、2
1.2 mol/(L·min) 1 mol/(L·min) 0.6 mol/(L·min) 0.4 mol/(L·min)
2、6、3、5 3、1、2、2 3、1、2、1 1、3、2、2
①为30 g ②为20 g ③为22.5 g ④为77.5 g
增大A.的浓度 增大容器的体积 加入催化剂 升高温度 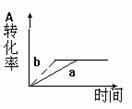

 p (g)+q (g),
p (g)+q (g), 若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图15所示,则对该反应的叙述正确的是( ) A.正反应是吸热反应B.逆反应是放热反应 C.m+n
若增大压强或升高温度,重新达到平衡,反应速率随时间的变化过程如图15所示,则对该反应的叙述正确的是( ) A.正反应是吸热反应B.逆反应是放热反应 C.m+n
 pC(g)+ qD(g)在一密闭容器中进行,测得平均反应速度vC.= 2v 。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是( ) A.2、6、3、5B.3、1、2、2 3、1、2、1 1、3、2、2
pC(g)+ qD(g)在一密闭容器中进行,测得平均反应速度vC.= 2v 。若反应达平衡后保持温度不变,加大体系压强时平衡不移动,则m、n、p、q的数值可以是( ) A.2、6、3、5B.3、1、2、2 3、1、2、1 1、3、2、2
