
 2C(s)+2O2(g)=2CO2(g),
2C(s)+2O2(g)=2CO2(g), C+O2=CO2,
C+O2=CO2,
 O2(g)=SO3(g);ΔH.=-315 kJ·mol-1 表示中和热的热化学方程式NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l); ΔH.=-57.3 kJ·mol-1 表示H2燃烧热的热化学方程式H2(g)+
O2(g)=SO3(g);ΔH.=-315 kJ·mol-1 表示中和热的热化学方程式NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l); ΔH.=-57.3 kJ·mol-1 表示H2燃烧热的热化学方程式H2(g)+ O2(g)=H2O(g);ΔH.=-241.8 kJ·mol-1 表示CO燃烧热的热化学方程式2CO(g)+O2(g)=2CO2(g);ΔH.=-566 kJ·mol-1
O2(g)=H2O(g);ΔH.=-241.8 kJ·mol-1 表示CO燃烧热的热化学方程式2CO(g)+O2(g)=2CO2(g);ΔH.=-566 kJ·mol-1

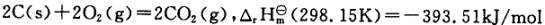 C(s)+O
C(s)+O (g)=COz(g)
(g)=COz(g) 