你可能感兴趣的试题
温度不变,增大容器的体积,S2Cl2的转化率降低 温度不变,缩小容器体积,液体的颜色加深 压强不变,升高温度,液体的颜色变浅 体积不变,降低温度,氯气的转化率降低
③、⑥中依次盛放浓硫酸、无水CaCl2 实验中需用酒精灯对④进行直接加热 实验过程中⑤冷凝回流的主要物质是S2Cl2 用减压分馏法从④中所得液体分离出S2Cl2
S2Cl2的结构式为Cl﹣S.﹣S.﹣Cl 反应中SO2是还原产物,S.是氧化产物 S2Cl2为含有极性键和非极性键的分子 反应中,生成1molSO2,转移电子为3mol
S2Cl2中每个原子都满足8电子稳定结构 S2Cl2是含有极性键和非极性键的极性分子 S2Br2与S2Cl2结构相似,熔点、沸点高低为:S2Cl2>S2Br2 与水反应的化学方程式可能为2S2Cl2+2H2O=SO2↑+3S↓+4HCl
橙黄色的澄明液体 无色澄明液体 淡黄色澄明油状液 红色澄明液体 黄色液体
橙黄色的澄明液体 无色澄明液体 浅黄色澄明油状液 红色澄明液体 黄色液体
S2Cl2的结构式为Cl-S.-S.-Cl S2Cl2为含有极性键和非极性键的非极性分子 S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2 S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
)单位时间里生成n mol S2Cl2的同时也生成n molCl2 ( )达到平衡时,若升高温度,压强不变,反应混合溶液颜色变浅 ( )达到平衡时,单位时间里消耗 n mol S2Cl2的同时也生成n molCl2 ( )加入氯气,平衡向正反应方向移动,氯气的转化率一定升高
S2Cl2中每个原子都满足8电子稳定结构 S2Cl2是含有极性键和非极性键的极性分子 S2Br2与S2Cl2结构相似,熔点、沸点高低为:S2Cl2>S2Br2 与水反应的化学方程式可能为2S2Cl2+2H2O=SO2↑+3S↓+4HCl
S2Br2与S2Cl2结构相似,沸点S2Br2 > S2Cl2 S2Cl2的结构式为Cl—S—S—Cl S2Cl2中S.显—1价 2S2Cl2+2H2O=SO2↑+3S↓+4HCl
S2Cl2分子中有极性键、非极性键 反应生成1molS,转移电子为3mol S2Cl2的结构式为:Cl-S-S-Cl S2Br2与S2Cl2结构相似,熔沸点S2Br2>S2Cl2
S2Cl2的结构式为Cl—S—S—Cl S2Cl2为含有极性键和非极性键的非极性分子 S2Br2与S2Cl2结构相似,熔、沸点:S2Br2>S2Cl2 S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
S2Cl2的电子式为 S2Br2与S2Cl2结构相似,熔、沸点:S2Br2>S2Cl2 S2Cl2为含有极性键和非极性键的非极性分子 S2Cl2与H2O反应的化学方程式可能为2S2Cl2+2H2O===SO2↑+3S↓+4HCl
S2Cl2中的硫元素显+1价 S2Cl2结构中的化学键只含有极性键 S2Br2与S2Cl2结构相似,其熔沸点:S2Br2>S2Cl2 S2Cl2与H2O反应的生成物中可能有S.
S2Cl2中的硫元素显+1价 S2Cl2结构中的化学键只含有极性键 S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2 S2Cl2与H2O反应的生成物中可能有S.
温度不变,增大容器的容积,S2Cl2的转化率降低
温度不变,缩小容器的容积,液体颜色加深
升高温度,压强不变,液体颜色变浅
降低温度,容积不变,Cl2的转化率降低
S2Cl2的结构式为Cl-S.-S.-Cl S2Cl2为含有极性键和非极性键的极性分子 S2Br2与S2Cl2结构相似,分子间作用力:S2Br2>S2Cl2 S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+4HCl 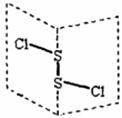
橙黄色的澄明液体 无色澄明液体 淡黄色澄明油状液体 红色澄明液体 黄色液体
S2Cl2晶体中不存在离子键 S2Cl2分子中各原子均达到8电子稳定结构 S2Cl2在液态下不能导电 S2Cl2与水反应后生成的气体通入石蕊试液中,现象是溶液先变红后褪色

