你可能感兴趣的试题
1L水中有1mol Na2SO4 1L溶液中含有142g Na2SO4 SO4 2-的物质的量浓度为2 mol/L 1LNa2SO4溶液中含有Na+ 1 mol
0.3 mol/L的Na2SO4溶液中含有Na+ 和SO42-的总物质的量为0.9 mol 当1 L.水吸收标准状况下的22.4 L.氯化氢时所得盐酸的浓度是1 mol/L 在K2SO4和NaCl的中性混合水溶液中,如果Na+ 和SO42-的物质的量相等,则K+ 和Cl—的物质的量浓度一定相同 10 ℃时,0.35 mol/L 的KCl饱和溶液100 mL蒸发掉5 g水,恢复到10 ℃时,它的物质的量浓度仍为0.35 mol/L
pH=12的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(OH-)相等 常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH) 常温下物质的量浓度相等的①NH4HCO3、②NH4HSO4、③NH4Fe(SO4)2:三种溶液中NH4+的浓度:②>③>① 等体积等物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数:N.前>N后
NaOH、Na2SO4、NaCl NaCl、NaOH、Na2SO4 NaCl、Na2SO4、NaOH Na2SO4、NaCl、NaOH
0.1 mol/L 0.15 mol/L 0.2 mol/L 0.25 mol/L
Na2SO4 和NaCl的物质的量之比为1 :3 溶液中一定有1molNa2SO4和3molNaCl 所带电荷数SO42-是Na+的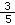 倍 SO42- 与Cl-的物质的量之和等于Na+的物质的量
倍 SO42- 与Cl-的物质的量之和等于Na+的物质的量
将溶液蒸干最多可以得到4 mol NaCl 将溶液蒸干并灼烧,得到的固体可能是NaCl、NaBr、Na2SO4 向溶液中滴加KI淀粉溶液,溶液变蓝,则氯气一定过量 若通入氯气的体积为11.2L.(标准状况),反应的离子方程式为:2I-+Cl2=I2+2C1-
K2SO4、BaCl2、NaNO3、NaCl HCl、(NH4)2SO4、Ba(OH)2、Na2SO4 KOH、Na2SO4、CuSO4、MgCl2 KCl、AgNO3、KNO3、NaCl
50mL 0.2mol·L-1的 NaCl 溶液 100mL 0.1mol·L-1的 NaCl 溶液 25mL 0.2mol·L-1的 Na2SO4 溶液 10mL 0.5mol·L-1的 Na2CO3 溶液
NaHSO3和NaHCO3的中性混合溶液中(S.和C.均用R.表示):c(Na+)=c(HRO3-)+2c(RO32-) 常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl―)>c(CH3COOH) 常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中c(NH4+):①<③<② 等体积等物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数多少:N.前后
溶液中可能含有0.5mol Na2SO4和1.5molNaCl SO42-离子和Cl-离子的物质的量之和等于Na+的物质的量 SO42-所带的电荷数是Na+所带的电荷数的3/5倍 Na2SO4和NaCl物质的量浓度之比为1:3
Na2CO3 NaHCO3 NaCl NH4Cl Na2CO3 NaHCO3 NH4Cl NaCl (NH4)2SO4 NH4Cl NaNO3 Na2S NH4Cl (NH4)2SO4 Na2S NaNO3
NaCl Na2SO4 NaBr Na2SO4 NaCl Na2SO4 I2 NaCl NaI Na2SO4

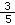 倍 SO42- 与Cl-的物质的量之和等于Na+的物质的量
倍 SO42- 与Cl-的物质的量之和等于Na+的物质的量