
 液中各离子浓度大小关系为: c(Na+)=c(SO42﹣)>c(NH4+)>c(H+)>c(OH﹣) 25℃ 时,将 a mo1•L﹣l 氨水与 0.01 moI•L﹣1 盐酸等体积 混合,反应完全时溶液中 c(NH4+)=c(C1﹣),用含a的 代数式表示NH3•H2O的电离常数Kb=
液中各离子浓度大小关系为: c(Na+)=c(SO42﹣)>c(NH4+)>c(H+)>c(OH﹣) 25℃ 时,将 a mo1•L﹣l 氨水与 0.01 moI•L﹣1 盐酸等体积 混合,反应完全时溶液中 c(NH4+)=c(C1﹣),用含a的 代数式表示NH3•H2O的电离常数Kb= 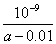 某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积V变化的 曲线如图所示。Ⅱ为醋酸稀释时pH的变化曲线,且a、b两点水的电离程度:a<b 已知298K时氢氰酸(HCN)的Ka=4.9×10﹣10、碳酸的Ka1=4.4×10﹣7,Ka2=4.7×10﹣11,据此可推测将氢氰酸加入到碳酸钠溶液中能观察到有气泡产生
某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积V变化的 曲线如图所示。Ⅱ为醋酸稀释时pH的变化曲线,且a、b两点水的电离程度:a<b 已知298K时氢氰酸(HCN)的Ka=4.9×10﹣10、碳酸的Ka1=4.4×10﹣7,Ka2=4.7×10﹣11,据此可推测将氢氰酸加入到碳酸钠溶液中能观察到有气泡产生
 c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
 液中各离子浓度大小关系为: c(Na+)=c(SO42﹣)>c(NH4+)>c(H+)>c(OH﹣) 25℃ 时,将 a mo1•L﹣l 氨水与 0.01 moI•L﹣1 盐酸等体积 混合,反应完全时溶液中 c(NH4+)=c(C1﹣),用含a的 代数式表示NH3•H2O的电离常数Kb=
液中各离子浓度大小关系为: c(Na+)=c(SO42﹣)>c(NH4+)>c(H+)>c(OH﹣) 25℃ 时,将 a mo1•L﹣l 氨水与 0.01 moI•L﹣1 盐酸等体积 混合,反应完全时溶液中 c(NH4+)=c(C1﹣),用含a的 代数式表示NH3•H2O的电离常数Kb= 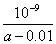 某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积V变化的 曲线如图所示。Ⅱ为醋酸稀释时pH的变化曲线,且a、b两点水的电离程度:a<b 已知298K时氢氰酸(HCN)的Ka=4.9×10﹣10、碳酸的Ka1=4.4×10﹣7,Ka2=4.7×10﹣11,据此可推测将氢氰酸加入到碳酸钠溶液中能观察到有气泡产生
某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积V变化的 曲线如图所示。Ⅱ为醋酸稀释时pH的变化曲线,且a、b两点水的电离程度:a<b 已知298K时氢氰酸(HCN)的Ka=4.9×10﹣10、碳酸的Ka1=4.4×10﹣7,Ka2=4.7×10﹣11,据此可推测将氢氰酸加入到碳酸钠溶液中能观察到有气泡产生