你可能感兴趣的试题
使用环形玻璃棒是为了加快反应速率,减小实验误差 为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 用0.5mol·L.-1NaOH溶液分别与0.5 mol·L.-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、滴定管、温度计
需要加热方能发生的反应不一定是吸热反应 反应是吸热还是放热取决于反应物和生成物所具有的总能量的相对大小 测定中和反应的反应热时,酸碱中和之后应读取体系达到的最高温度 硫在氧气中燃烧,该反应反应产物的总焓大于反应物的总焓
在化学反应过程中所放出或吸收的热量称为反应热 在稀溶液中,1mol酸跟1mol碱发生中和反应所放出的热量叫做中和热 对于吸热反应,反应物所具有的总能量总是低于生成物所具有的总能量 在101kPa,1mol物质完全燃烧生成稳定氧化物时所放出的热量叫做该物质的燃烧热
为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 用0.5mol/LNaOH溶液分别与0.5mol/L的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 使用环形玻璃搅拌棒可使反应物混合均匀,加快反应速率,减小实验误差 在测定中和热实验中需要使用的仪器包括:天平、量筒、烧杯、环形玻璃搅拌棒
实验需用到的主要玻璃仪器包括大、小烧杯,温度计,环形玻璃搅拌棒及泡沫塑料板、碎泡沫塑料(或硬纸板、碎纸条)等; 盐酸与某强碱中和放出的热量随反应物的用量改变而改变,但中和热不变; NaOH稍过量的目的是保证盐酸完全被NaOH中和; 测定结果准确与否的关键是尽量减小热量损失及准确读取混合溶液的最高温度等。
使用环形玻璃搅拌棒是为了加大反应速率,减小实验误差 为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 用0.5mol·L.-1NaOH溶液分别与0.5mol·L.-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、滴定管、温度计
化学反应的反应热都可以通过实验测定出来 活化能越大的化学反应其反应热数值也越大 反应热的产生是由于生成物与反应物的总能量不同 放热反应是由于反应物键能总和大于生成物键能总和
使用环形玻璃棒是为了加快反应速率,减小实验误差 为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触 用0.5mol·L-1NaOH溶液分别与0.5 mol·L-1的盐酸、醋酸溶液反应,如所取的溶液体积 相等,则测得的中和热数值相同 在测定中和热实验中需要使用的仪器有:天平、量筒、烧杯、滴定管、温度计
已经转化的某反应物的量与反应前该反应物的量之比 反应前该反应物的量与已经转化的某反应物的量之比 反应物的平衡浓度与反应物的起始浓度之比 反应物的平衡物质的量与反应物的起始物质的量之比
实验需用到的主要玻璃仪器包括大、小烧杯,温度计,环形玻璃搅拌棒及泡沫塑料板、碎泡沫塑料(或硬纸板、碎纸条)等; 盐酸与某强碱中和放出的热量随反应物用量的改变而改变,但中和热不变; NaOH稍过量的目的是保证盐酸完全被NaOH中和; 测定结果准确与否的关键是尽量减小热量损失及准确读取混合溶液的最高温度等。
点以前和以后反应速率的限制因素是 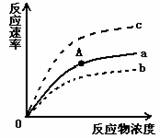 A.酶量和反应物浓度 反应物浓度和酶量 反应物浓度和反应物浓度 酶量和酶量
A.酶量和反应物浓度 反应物浓度和酶量 反应物浓度和反应物浓度 酶量和酶量
在化学反应进行的过程中放出或吸收的热量称为反应热。
在稀溶液中,1mol酸跟1mol碱发生中和反应所放出的热量叫做中和热。
对于吸热反应,反应物所具有的总能量总是低于生成物所具有的总能量。
在101Kpa时,1mol物质完全燃烧生成稳定氧化物时,所放出的热量叫做该物质的燃烧热。

 A.酶量和反应物浓度 反应物浓度和酶量 反应物浓度和反应物浓度 酶量和酶量
A.酶量和反应物浓度 反应物浓度和酶量 反应物浓度和反应物浓度 酶量和酶量