你可能感兴趣的试题
反应物和生成物中只有1种单质 NH3 的水溶液pH大于7 反应中有2种元素的化合价变化了 反应物和生成物中有2种氧化物
图中有两种单质和两种氧化物 反应物和生成物均含有毒气体 生成单质与化合物的质量比为7:22 生成物的分子个数比为1:1
NO FeSO4 Fe(NO3)3 Fe2(SO4)3
该容器中发生了氧化还原反应 该反应中HNO3、H2O等物质是反应物,H2SO4、NO、H3AsO4是生成物 HNO3、H2SO4、H3AsO4都属于最高价氧化物的水化物 该反应中只有砷元素被氧化、只有氮元素被还原
若有l mol NO3-参加还原反应,则转移8mol e- 还原产物为NH4+ 氧化剂与还原剂的物质的量之比为8:l 若把该反应设计为原电池,则负极反应为Fe 2+ -e-=Fe 3+
该反应属于氧化还原反应 HNO3、H2O是反应物,H2SO4、NO、H3AsO4是生成物 此反应中只有砷元素被氧化,只有氮元素被还原 HNO3、H2SO4、H3AsO4都是最高价氧化物对应的水化物
还原产物为NH4+ 氧化剂与还原剂的物质的量之比为1:8 Fe3+和Fe2+分别属于反应物和生成物 若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+
氧化剂与还原剂的物质的量之比为1:8 该过程说明 溶液不宜加酸酸化 若有
溶液不宜加酸酸化 若有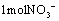 发生氧化反应,则转移8
发生氧化反应,则转移8 电子 若把该反应设计为原电池,则负极反应为
电子 若把该反应设计为原电池,则负极反应为
氧化剂与还原剂的物质的量之比为8∶1 还原产物为NH4+ 若有1 mol NO3-参加还原反应,则转移8mol e- 若把该反应设计为原电池,则负极反应为Fe2+—e-= Fe3+
氧化剂与还原剂的物质的量之比为1:8 还原产物为NH4+ 若有1 mol NO3﹣参加还原反应,转移8 mol e﹣ 若把该反应设计为原电池,则正极反应为Fe2+﹣e﹣═Fe3+
还原产物为NH4+ 若有1mol NO3-参加还原反应,则转移8mole- 氧化剂与还原剂的物质的量之比为8∶1 若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+

 溶液不宜加酸酸化 若有
溶液不宜加酸酸化 若有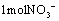 发生氧化反应,则转移8
发生氧化反应,则转移8 电子 若把该反应设计为原电池,则负极反应为
电子 若把该反应设计为原电池,则负极反应为