
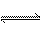
 C.(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是 ①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量④B物质的量浓度 A.①④ ②③ ②③④ 只有④
C.(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是 ①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量④B物质的量浓度 A.①④ ②③ ②③④ 只有④
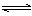 C.(g)+D.(g),当下列物理量不发生变化时,能说明该反应已达到平衡状态的是( ) ①混合气体的密度 ②容器内气体的压强 ③混合气体总物质的量 ④ 的物质的量浓度 A.①④B.只有②③ ②③④ 只有④
C.(g)+D.(g),当下列物理量不发生变化时,能说明该反应已达到平衡状态的是( ) ①混合气体的密度 ②容器内气体的压强 ③混合气体总物质的量 ④ 的物质的量浓度 A.①④B.只有②③ ②③④ 只有④
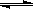 C.(g)+D.(g)已达平衡的是( )
C.(g)+D.(g)已达平衡的是( ) C.(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是( )①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量 ④ 的物质的量浓度A.①④B.②③ ②③④ 只有④
C.(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是( )①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量 ④ 的物质的量浓度A.①④B.②③ ②③④ 只有④
 2C(g), 当下列物理量不发生变化时,能表明该反应已达到平衡状态的是( ) ①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量 ④ 物质的量浓度 A.①②④ B.②③ ②③④ 全部
2C(g), 当下列物理量不发生变化时,能表明该反应已达到平衡状态的是( ) ①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量 ④ 物质的量浓度 A.①②④ B.②③ ②③④ 全部
 C.(g)+D(g)已达到平衡状态的是 ()。
C.(g)+D(g)已达到平衡状态的是 ()。 C.(g)+D(l),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是 ①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量④ 的物质的量浓度 A.①②④B.②③ ②③④ 只有④
C.(g)+D(l),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是 ①混合气体的密度 ②容器内气体的压强 ③混合气体的总物质的量④ 的物质的量浓度 A.①②④B.②③ ②③④ 只有④
 C(g)+D.(g)已达平衡的是( ) A. 混合气体的压强 混合气体的密度 A.的物质的量浓度 气体总物质的量
C(g)+D.(g)已达平衡的是( ) A. 混合气体的压强 混合气体的密度 A.的物质的量浓度 气体总物质的量
 C.(g)+D.(g),当下列物理量不发生变化时,能说明该反应已达到平衡状态的是( ) ①混合气体的密度 ②容器内气体的压强 ③混合气体总物质的量 ④B物质的量浓度 A.①④ 只有②③ ②③④ 只有④
C.(g)+D.(g),当下列物理量不发生变化时,能说明该反应已达到平衡状态的是( ) ①混合气体的密度 ②容器内气体的压强 ③混合气体总物质的量 ④B物质的量浓度 A.①④ 只有②③ ②③④ 只有④
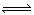
 C.(g)+D.(g),当下列物理量不发生变化时,能说明该反应已达到平衡状态的是( ) ①混合气体的密度 ②容器内气体的压强 ③混合气体总物质的量 ④B物质的量浓度 A.①④ 只有②③ ②③④ 只有④
C.(g)+D.(g),当下列物理量不发生变化时,能说明该反应已达到平衡状态的是( ) ①混合气体的密度 ②容器内气体的压强 ③混合气体总物质的量 ④B物质的量浓度 A.①④ 只有②③ ②③④ 只有④
 C.(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的有( ) ①混合气体的密度②容器内气体的压强③混合气体的总物质的量④C.物质的量浓度 ⑤混合气体的平均相对分子质量 ⑥ 的转化率 A.①④⑤⑥B.④⑤⑥ ②③④ ④⑥
C.(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的有( ) ①混合气体的密度②容器内气体的压强③混合气体的总物质的量④C.物质的量浓度 ⑤混合气体的平均相对分子质量 ⑥ 的转化率 A.①④⑤⑥B.④⑤⑥ ②③④ ④⑥