你可能感兴趣的试题
X.与Y.可形成YX2型化合物 离子半径 X >Z. 最高价氧化物对应水化物的酸性 Y>Z 气态氢化物的稳定性 X> Y
B.C.D.,原子序数依次增大;A.C.的原子序数的差为8,A. C.三种元素原子的最外层电子数之和为15,B.原子最外层电子数等于A.原子最外层电子数的一半。下列叙述正确的是( ) A.原子半径:A.<B.< <DB.非金属性:A.>C. C.最高价氧化物对应水化物的酸性: <CD.单质B.在常温下能溶于浓硝酸
元素性质随着核外电子周期性的排布而呈周期性的变化 同一周期的元素的第一电离能随着原子序数的递增,由小到大 同一周期的元素的原子电负性随着原子序数的递增,由小到大 同一周期的元素的原子半径随着原子序数的递增,由大到小 同一周期的元素的主要化合价随着原子序数的递增,由小到大
原子半径:甲<乙<丙 最外层电子数:丙>丁 若甲、乙、丙均是金属,则氢氧化物碱性:甲<乙<丙 若乙的最高价含氧酸为强酸,则丙是活泼非金属元素
元素④的原子序数小于元素⑦的原子序数 ②、③处于同一周期 上述八种元素最高价氧化物对应的水化物中,⑤号酸性最强 ⑧号元素原子结构示意图为: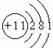
B.C.D.,原子序数依次增大。A.C.的原子序数的差为8,A. C.三种元素原子的最外层电子数之和为15,B.原子最外层电子数等于A.原子最外层电子数的一半。下列叙述正确的是( ) A.原子半径:A.<B.< <DB.非金属性:C.>A. C.最高价氧化物对应水化物的酸性: >CD.单质B.常温下能溶于浓硝酸
114号元素位于第七周期第ⅣA族 原子序数之差为2的两种元素可能位于同一主族 同一主族的甲乙两种元素,甲的原子序数为x,则乙的原子序数可能为x+32 同一周期的甲乙两种元素,甲位于ⅠA族,原子序数为x,乙位于ⅢA族,则乙原子序数可能为x+19
最外层有5个电子的原子都是非金属原子 最外层有2个电子的原子都是金属原子 非金属元素的最高正化合价与负化合价的绝对值之和均等于8 同一短周期ⅡA族元素与ⅢA族元素的原子序数一定相差1
同主族元素随原子序数递增,元素原子的得电子能力逐渐增强 同主族元素随原子序数递增,单质氧化能力逐渐减弱 同主族元素原子最外层电子数都相同 同主族元素的原子半径,随原子序数增大而逐渐增大
单质的化学活泼性:W.<X.<Y.<Z. 最外层电子数:W.<X.<Y.<Z. 单质的氧化能力:W.<X.<Y.<Z. 元素的最高化合价:W.<X.<Y.<Z.
元素性质随着核外电子周期性的排布而呈周期性的变化 同一周期的元素的第一电离能随着原子序数的递增,由小到大 同一周期的元素的原子半径随着原子序数的递增,由大到小 同一周期的元素的原子电负性随着原子序数的递增,由小到大 同一周期的元素的主要化合价随着原子序数的递增,由小到大
B.C.D.,原子序数依次增大。A.C.的原子序数的差为8,A. C.三种元素原子的最外层电子数之和为15,B.原子最外层电子数等于A.原子最外层电子数的一半。下列叙述正确的是 A.原子半径:A.<B.< <DB.单质B.常温下能溶于浓硝酸 C.最高价氧化物对应水化物的酸性: <CD.非金属性:A.>C.
单质的化学活泼性:W<X<Y<Z 原子最外层电子数:W<X<Y<Z 单质的氧化能力:W<X<Y<Z 元素的最高化合价:W<X<Y<Z
B.C.D.的原子序数依次增大,A.C.原子序数相差8,A原子的最外层电子数是其次外层电子数的3倍,在同周期主族元素中 的原子半径最大。下列说法正确的是 A.氢化物的热稳定性:A元素B.与 形成的化合物是离子化合物 D.最高价氧化物对应的水化物的酸性:C>D
第ⅠA.族元素单质的熔点随着原子序数递增而升高 卤族元素单质的熔点随着原子序数递增而升高 第ⅤA.族元素的气态氢化物沸点随着原子序数递增而升高 第三周期元素形成的简单离子半径随着原子序数递增而增大