你可能感兴趣的试题
还原性:I- >Fe2+ > Br- 原混合溶液中FeBr2的物质的量为6mol 当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
原混合溶液中FeBr2的物质的量为6mol 当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
通入氯气后的溶液中一定不存在I.- 通入氯气之后原溶液中的Fe2+全部被氧化 原溶液中的Br-可能被氧化 若取少量所得溶液,再加入CCl4溶液充分振荡,静置、分液,下层溶液可能呈紫红色
线段BD表示Fe3+物质的量的变化 原混合溶液中FeBr2的物质的量为6 mol 当通入2 mol Cl2时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- 原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3
通入氯气后的溶液中一定不存在I.-; 通入氯气之后原溶液中的Fe2+全部被氧化; 原溶液中的Br-可能被氧化; 若取少量所得溶液,再加入CCl4溶液充分振荡,静置、分液,下层 溶液可能呈紫红色
通入氯气后的溶液中一定不存在I.﹣ 通入氯气之后原溶液中的Fe2+全部被氧化 原溶液中的Br﹣可能被氧化 若取少量所得溶液,再加入CCl4溶液充分振荡,静置、分液,下层溶液可能呈紫红色
线段BD表示Fe3+物质的量的变化 原混合溶液中FeI2的物质的量为1mol 当通入2 mol Cl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- 原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶3∶1
还原性:I- >Fe2+ > Br- 原混合溶液中FeBr2的物质的量为6mol 当通入2molCl2时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3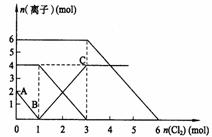
还原性:I- >Fe2+ > Br- 原混合溶液中FeBr2的物质的量为6mol 当通入2molCl2时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
通入氯气后的溶液中一定不存在I.-; 通入氯气之后原溶液中的Fe2+全部被氧化; 原溶液中的Br-可能被氧化; 若取少量所得溶液,再加入CCl4溶液充分振荡,静置、分液,下层溶液呈紫红色
氧化性:Cl2>Fe3+>Br2>I2 ②发生反应Fe2++Cl2=Fe3++2Cl- 实验中只有氯气发生氧化反应 实验②发生的反应中,有一个是非氧化还原反应
原溶液中的Br-不一定被氧化 通入氯气之后原溶液中的Fe2+一定被氧化 不能确定通入氯气之后的溶液中是否存在Fe2+ 若取少量所得溶液,再加入CCl4溶液,静置、分液,向上层溶液中加入足量的AgNO3溶液,能产生黄色沉淀
浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气后都首先发生置换反应 XCl3的溶液能与铜片发生反应,则铜的金属性一定比X.强 非金属X.能将Fe氧化到+3价,但非金属Y.不能,则Y.的氧化性一定比X.强 Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化
向Na2CO3饱和溶液中通入过量CO2,有NaHCO3结晶析出 向FeSO4溶液中通入过量CO2,有浑浊现象产生 SO2具有漂白性,常用于自来水消毒 Fe和Br2混合加热生成FeBr2 
还原性:I.->Fe2+>Br- 原混合溶液中FeBr2的物质的量为6 mol 当通入2 mol Cl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- 原溶液中:n(Fe2+)∶ n(I-)∶ n(Br-)=2∶ 1∶ 3

 原混合溶液中FeBr2的物质的量为6mol 当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
原混合溶液中FeBr2的物质的量为6mol 当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3



