你可能感兴趣的试题
-1940kJ·mol-1 1940kJ·mol-1 -485kJ·mol-1 485kJ·mol-1
485.5 kJ/mol 610 kJ/mol 917 kJ/mol 1220 kJ/mol
P—P键的键能大于P—Cl键的键能 可求Cl2(g)+ PCl3(g)===PCl5(s)的反应热ΔH. Cl—Cl键的键能为(b-a+5.6c)/4 kJ·mol-1 P—P键的键能为(5a-3b+12c)/8 kJ·mol-1
-183 kJ·mol-1 183 kJ·mol-1 -862 kJ·mol-1 862 kJ·mol-1
+1638kJ・mol-1 -1638kJ・mol-1 -126kJ・mol-1 +126kJ・mol-1
P—P键的键能大于P—Cl键的键能 可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH Cl—Cl键的键能为(b-a+5.6c)/4 kJ·mol-1 P—P键的键能为(5a-3b+12c)/8 kJ·mol-1
(x+y-Q)kJ・mol-1 (x+y+Q)kJ・mol-1
 kJ・mol-1
kJ・mol-1 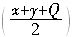 kJ・mol-1
kJ・mol-1
862kJ/mol 183kJ/mol ﹣862kJ/mol ﹣183kJ/mol
P.-P.键的键能大于P.-Cl键的键能 可求Cl2(g)+ PCl3(g)===4PCl5(g)的反应热ΔH. Cl-Cl键的键能为(b-a+5.6c)/4 kJ·mol-1 P.-P.键的键能为(5a-3b+12c)/8 kJ·mol-1
CO 的燃烧热是 283. 0 kJ/mol,则2CO2(g) =2CO(g)+O2(g) ΔH=+283.0 kJ/mol HC1和NaOH反应的中和热ΔH=-57. 3 kJ/mol,则H2SO4和Ba(OH)2的反应热ΔH=2×(-57.3) kJ/mol 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量少 已知:H—H键的键能为a kJ/mol,Cl—C1键的键能为b kJ/mol,H—C1键的键能为c kJ/mol,则生成1 mol HC1放出的能量为(a+b-2c)/2 kJ
431kJ·mol-1 945.6kJ·mol-1 649kJ·mol-1 896kJ·mol-1
﹣183 kJ/mol 183 kJ/mol ﹣862 kJ/mol 862 kJ/mol
CO的燃烧热是283.0 kJ/mol,则2CO2(g) 2CO(g)+O2(g) ΔH.=+283.0 kJ/mol HCl和NaOH反应的中和热ΔH.=-57.3 kJ/mol,则H.2SO4和Ba(OH)2的反应热ΔH.=2×(-57.3) kJ/mol 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量少 已知:H.-H.键的键能为a kJ/mol,Cl-Cl键的键能为b kJ/mol,H.-Cl键的键能为c kJ/mol,则生成1 mol HCl放出的能量为(a+b-2c)/2 kJ
2CO(g)+O2(g) ΔH.=+283.0 kJ/mol HCl和NaOH反应的中和热ΔH.=-57.3 kJ/mol,则H.2SO4和Ba(OH)2的反应热ΔH.=2×(-57.3) kJ/mol 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量少 已知:H.-H.键的键能为a kJ/mol,Cl-Cl键的键能为b kJ/mol,H.-Cl键的键能为c kJ/mol,则生成1 mol HCl放出的能量为(a+b-2c)/2 kJ
496 kJ·mol-1 431 kJ·mol-1 862 kJ·mol-1 248 kJ·mol-1
P.-P.键的键能大于P.-Cl键的键能 可求Cl2(g)+ PCl3(g)=4PCl5(s)的反应热△H. Cl-Cl键的键能为(b-a+5.6c)/4 kJ∙mol—1 P.-P.键的键能为(5a-3b+12c)/8 kJ∙mol—1
1/2H2(g)+ 1/2Cl2(g)=HCl(g);△H=-91.5 kJ・mol-1 H2(g)+ Cl2(g)=2HCl(g); △H=-183 kJ・mol-1 1/2H2(g)+ 1/2Cl2(g)=HCl(g);△H=+91.5 kJ・mol-1 2HCl(g)= H2(g)+ Cl2(g); △H=+183kJ・mol-1

 kJ・mol-1
kJ・mol-1 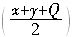 kJ・mol-1
kJ・mol-1
 2CO(g)+O2(g) ΔH.=+283.0 kJ/mol HCl和NaOH反应的中和热ΔH.=-57.3 kJ/mol,则H.2SO4和Ba(OH)2的反应热ΔH.=2×(-57.3) kJ/mol 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量少 已知:H.-H.键的键能为a kJ/mol,Cl-Cl键的键能为b kJ/mol,H.-Cl键的键能为c kJ/mol,则生成1 mol HCl放出的能量为(a+b-2c)/2 kJ
2CO(g)+O2(g) ΔH.=+283.0 kJ/mol HCl和NaOH反应的中和热ΔH.=-57.3 kJ/mol,则H.2SO4和Ba(OH)2的反应热ΔH.=2×(-57.3) kJ/mol 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量少 已知:H.-H.键的键能为a kJ/mol,Cl-Cl键的键能为b kJ/mol,H.-Cl键的键能为c kJ/mol,则生成1 mol HCl放出的能量为(a+b-2c)/2 kJ