你可能感兴趣的试题
该溶液lmL稀释至100mL后,pH等于3 向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和 该溶液中硝酸电离出的c(H++H.)与水电离出c(H++H.)的之比值为10-12 该溶液中水电离出的c(H++H.)是pH为3的硝酸中水电离出的c(H++H.)的100倍
该溶液1 mL稀释至100 mL后,pH小于3 向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和 该溶液中硝酸电离出的c(H+)与水电离出的c(H+)的比值为10-12 该溶液中水电离出c(H+)是pH为3的硝酸中水电离出c(H+)的100倍
该溶液1 mL稀释至100 mL后,pH小于3 向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和 该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为10-12 该溶液中水电离出c(H+)是pH为3的硝酸中水电离出c(H+)的100倍
点表示25℃时水的电离达平衡时的离子浓度, 点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是  A.纯水中25℃时的c(H+)比100℃时的c(H+)大 B.100℃时某溶液中由水电离产生的c(H+)=1×10-11mol/L,则该溶液的pH可能是11或3 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某Na2SO4 溶液中c(SO42-)=5×10-4 mol/L,则溶液中c(Na+):c(OH-)为104:1
A.纯水中25℃时的c(H+)比100℃时的c(H+)大 B.100℃时某溶液中由水电离产生的c(H+)=1×10-11mol/L,则该溶液的pH可能是11或3 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某Na2SO4 溶液中c(SO42-)=5×10-4 mol/L,则溶液中c(Na+):c(OH-)为104:1
点表示25°C时水的电离达平衡时的离子浓度, 点表示1000 时水的电离达平衡时的离子浓度, 则下列说法正确的是 ( ) A.纯水中25°C时的,c(H+)比100℃ 的时c(H+)大B.1000C.时某溶液中由水电离产生的c(H+)=1×10-11mol·L-1,则该溶液的pH可能是11或3C.将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持1000C.的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某NaSO2SO4溶液中c(SO22-4)=5×10-4mol/L,则溶液中c(Na+):c(OH-)为104:1
则下列说法正确的是 ( ) A.纯水中25°C时的,c(H+)比100℃ 的时c(H+)大B.1000C.时某溶液中由水电离产生的c(H+)=1×10-11mol·L-1,则该溶液的pH可能是11或3C.将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持1000C.的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某NaSO2SO4溶液中c(SO22-4)=5×10-4mol/L,则溶液中c(Na+):c(OH-)为104:1
该溶液1 mL稀释至100 mL后,pH等于2 向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和 该溶液中硝酸电离出的c(H.+)与水电离出的c(H.+)之比值为10-12 该溶液中水电离出的c(H.+)是pH为3的硝酸中水电离出的c(H.+)的100倍
c(H.+)·c(OH-)乘积增大 溶液pH增大 c(OH-)降低了 水电离出的c(H.+)增加了
将10 mL该溶液稀释至100 mL后,pH小于3 向该溶液中加入等体积pH为12的氨水恰好完全中和 该溶液中酸电离出的c(H+)与水电离出的c(H+)之比为1010∶1 该溶液中由水电离出的c(H+)水·c(OH-)水=1×10-14
点表示25 ℃时水  的电离达平衡时的离子浓度, 点表示100 ℃时水的 电离达平衡时的离子浓度, 则下列说法正确的是( ) A.纯水中25 ℃时的c(H+)比100 ℃时的c(H+)大 B.100 ℃时某溶液中由水电离产生的c(H+)=1×10-11 mol·L-1,则该溶液的pH可能是11或3 25 ℃时,某Na2SO4溶液中c(SO
的电离达平衡时的离子浓度, 点表示100 ℃时水的 电离达平衡时的离子浓度, 则下列说法正确的是( ) A.纯水中25 ℃时的c(H+)比100 ℃时的c(H+)大 B.100 ℃时某溶液中由水电离产生的c(H+)=1×10-11 mol·L-1,则该溶液的pH可能是11或3 25 ℃时,某Na2SO4溶液中c(SO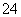 )=5×10-4 mol·L-1,则溶液中c(Na+)∶c(OH-)为104∶1 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100 ℃的恒温,混合溶液的pH =7,则Ba(OH)2溶液和盐酸的体积比为10∶1
)=5×10-4 mol·L-1,则溶液中c(Na+)∶c(OH-)为104∶1 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100 ℃的恒温,混合溶液的pH =7,则Ba(OH)2溶液和盐酸的体积比为10∶1
该溶液1 mL稀释至100 mL后,pH大于3 向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和 该溶液中硝酸电离出的[H+]与水电离出的[H+]的比值为10-12 该溶液中水电离出的[H+]是pH为3的硝酸中水电离出的[H+]的100倍
点表示25℃时水的电离达平衡时的离子浓度, 点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是  A.纯水中25℃时的c(H+)比100℃时的c(H+)大 B.100℃时某溶液中由水电离产生的c(H+)=1×10-11mol/L,则该溶液的pH可能是11或3 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某Na2SO4 溶液中c(SO42-)=5×10-4 mol/L,则溶液中c(Na+):c(OH-)为104:1
A.纯水中25℃时的c(H+)比100℃时的c(H+)大 B.100℃时某溶液中由水电离产生的c(H+)=1×10-11mol/L,则该溶液的pH可能是11或3 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某Na2SO4 溶液中c(SO42-)=5×10-4 mol/L,则溶液中c(Na+):c(OH-)为104:1
a2<a3<a1<a4 a3=a2<a1<a4 a2=a3<a4<a1 a1<a2<a3<a4

 A.纯水中25℃时的c(H+)比100℃时的c(H+)大 B.100℃时某溶液中由水电离产生的c(H+)=1×10-11mol/L,则该溶液的pH可能是11或3 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某Na2SO4 溶液中c(SO42-)=5×10-4 mol/L,则溶液中c(Na+):c(OH-)为104:1
A.纯水中25℃时的c(H+)比100℃时的c(H+)大 B.100℃时某溶液中由水电离产生的c(H+)=1×10-11mol/L,则该溶液的pH可能是11或3 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某Na2SO4 溶液中c(SO42-)=5×10-4 mol/L,则溶液中c(Na+):c(OH-)为104:1
 则下列说法正确的是 ( ) A.纯水中25°C时的,c(H+)比100℃ 的时c(H+)大B.1000C.时某溶液中由水电离产生的c(H+)=1×10-11mol·L-1,则该溶液的pH可能是11或3C.将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持1000C.的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某NaSO2SO4溶液中c(SO22-4)=5×10-4mol/L,则溶液中c(Na+):c(OH-)为104:1
则下列说法正确的是 ( ) A.纯水中25°C时的,c(H+)比100℃ 的时c(H+)大B.1000C.时某溶液中由水电离产生的c(H+)=1×10-11mol·L-1,则该溶液的pH可能是11或3C.将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持1000C.的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某NaSO2SO4溶液中c(SO22-4)=5×10-4mol/L,则溶液中c(Na+):c(OH-)为104:1
 的电离达平衡时的离子浓度, 点表示100 ℃时水的 电离达平衡时的离子浓度, 则下列说法正确的是( ) A.纯水中25 ℃时的c(H+)比100 ℃时的c(H+)大 B.100 ℃时某溶液中由水电离产生的c(H+)=1×10-11 mol·L-1,则该溶液的pH可能是11或3 25 ℃时,某Na2SO4溶液中c(SO
的电离达平衡时的离子浓度, 点表示100 ℃时水的 电离达平衡时的离子浓度, 则下列说法正确的是( ) A.纯水中25 ℃时的c(H+)比100 ℃时的c(H+)大 B.100 ℃时某溶液中由水电离产生的c(H+)=1×10-11 mol·L-1,则该溶液的pH可能是11或3 25 ℃时,某Na2SO4溶液中c(SO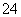 )=5×10-4 mol·L-1,则溶液中c(Na+)∶c(OH-)为104∶1 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100 ℃的恒温,混合溶液的pH =7,则Ba(OH)2溶液和盐酸的体积比为10∶1
)=5×10-4 mol·L-1,则溶液中c(Na+)∶c(OH-)为104∶1 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100 ℃的恒温,混合溶液的pH =7,则Ba(OH)2溶液和盐酸的体积比为10∶1
 A.纯水中25℃时的c(H+)比100℃时的c(H+)大 B.100℃时某溶液中由水电离产生的c(H+)=1×10-11mol/L,则该溶液的pH可能是11或3 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某Na2SO4 溶液中c(SO42-)=5×10-4 mol/L,则溶液中c(Na+):c(OH-)为104:1
A.纯水中25℃时的c(H+)比100℃时的c(H+)大 B.100℃时某溶液中由水电离产生的c(H+)=1×10-11mol/L,则该溶液的pH可能是11或3 将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1 25℃时,某Na2SO4 溶液中c(SO42-)=5×10-4 mol/L,则溶液中c(Na+):c(OH-)为104:1