你可能感兴趣的试题
化合物KCrO2中Cr元素为+3价 实验①证明Cr2O3是两性氧化物 实验②证明氧化性:Cr2O72﹣>I2 实验③证明H2O2既有氧化性又有还原性
化合物KCrO2中Cr元素为+3价 实验①证明Cr2O3是两性氧化物 实验②证明氧化性:Cr2O72->I2 实验③证明H2O2既有氧化性又有还原性
[Mn]+[O]=(MnO) [Mn]+(1/2){O2}=(MnO) [Mn]+(FeO)=(MnO)+[Fe] 3[Mn]+(Cr2O3)=3(MnO)+2[Cr]
CaO、MnO、FeO P2O5、TiO2、V2O5 Al2O3、Fe2O3、Cr2O3
化合物KCrO2中Cr元素为+1价 实验①证明Cr2O3是酸性氧化物 实验②证明H2O2既有氧化性又有还原性 实验③证明氧化性:Cr2O72-> I2
AlO3、Cr2O3、Fe2O3 CaO、MnO、FeO SiO2、TiO2、SO2
实验①证明Cr2O3是两性氧化物 实验②中H2O2是氧化剂,K2Cr2O7是氧化产物 实验③证明氧化性:Cr2O72->I- 实验③中,若生成1.27gI2,则反应中转移0.01mol电子
化合物KCrO2中Cr元素为+3价 实验①证明Cr2O3是两性氧化物 实验②证明氧化性:Cr2O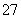 >I2 实验③证明H2O2既有氧化性又有还原性
>I2 实验③证明H2O2既有氧化性又有还原性
化合物KCrO2中Cr元素为+3价 实验①证明Cr2O3是两性氧化物 实验②证明H2O2既有氧化性又有还原性 实验③证明氧化性:Cr2O72- > I2
反应(1)和(2)均为氧化还原反应 反应(1)的氧化剂是O2,还原剂是FeO·Cr2O3 高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4 反应(1)中每生成1molNa2CrO4时电子转移3mol
①中溶液橙色加深,③中溶液变黄 ②中Cr2O72-被 2H5OH还原 C.对比②和④可知K2Cr2O7酸性溶液氧化性强 若向④中加入70%H2SO4溶液至过量,溶液变为橙色
化合物KCrO2中Cr元素为+3价 实验①证明Cr2O3是两性氧化物 实验②证明氧化性:Cr2O >I2 实验③证明H2O2既有氧化性又有还原性
>I2 实验③证明H2O2既有氧化性又有还原性

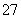 >I2 实验③证明H2O2既有氧化性又有还原性
>I2 实验③证明H2O2既有氧化性又有还原性
 >I2 实验③证明H2O2既有氧化性又有还原性
>I2 实验③证明H2O2既有氧化性又有还原性