你可能感兴趣的试题
Zn(s)+Ag2O(s)=ZnO(s)+2Ag(s) ΔH.=+317.3kJ·mol-1 Zn+Ag2O=ZnO+2Ag ΔH.=+317.3kJ·mol-1 Zn(s)+Ag2O(s)=ZnO(s)+2Ag(s) ΔH.=-317.3kJ 2Zn(s)+2Ag2O(s)=2ZnO(s)+4Ag(s) ΔH.=-634.6 kJ·mol-1
ag硫和bg氧气完全反应生成cg二氧化硫,则a+b≥c
ag镁与bg稀硫酸充分反应后所得的溶液质量为cg,则a+b>c
ag硝酸钾饱和溶液中加入bg硝酸钾固体能得到cg硝酸钾溶液,则a=c
已知:A+2B=C,其中反应前A与B的质量分别为ag和bg,反应后C的质量为cg,则a+b=c
M.的金属活动性比Ag强 金属M.可能是铜 该反应可能是置换反应 该反应前后M.的化合价发生了改变
2C O (g)+ O2(g)==2CO2(g) HNO3(aq)+NaOH(aq)==NaNO3(aq)+H2O(l) 2H2(g)+O2(g)==2H2O(l) Zn(s)+ Ag2 O(s)== Zn O(s)+2Ag(s)
该反应属于置换反应 金属M.可能是铝 M.的金属活动性比Ag强 反应前后M.的化合价改变
该装置为原电池 Ag电极质量增加,铜逐渐溶解 反应一段时间后左池中NO3-浓度变大 总反应为:Cu(s)+2Ag+(aq)=Cu2+ (aq)+ 2Ag (s)
M.的金属活动性比Ag强 金属M.可能是铜 该反应属于复分解反应 该反应前后M.的化合价发生了改变
M.的金属活动性比Ag强 金属M.不可能是铜 ( ) 该反应属于复分解反应 该反应前后M.的化合价发生了改变
2H2S + SO2 = 3S↓ + 2H2O (复分解反应) CO2 +  2CO (化合反应) C. 2AgBr
2CO (化合反应) C. 2AgBr 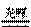 2Ag + Br2↑(分解反应) 2Mg + CO2
2Ag + Br2↑(分解反应) 2Mg + CO2  2MgO +C.(置换反应)
2MgO +C.(置换反应)
Zn(s)十Ag2O(s)====ZnO(s)+2Ag(s),△H=317.3kJ/mol Zn+Ag2O=====ZnO+2Ag,△H=317.3kJ/mol Zn(s)+Ag2O(s)=====ZnO(s)+2Ag(s),△H=-317.3kJ/mol 2Zn(s)+2Ag2O(s)=====2ZnO(s)+4Ag(s),△H=-317.3kJ
Y.为CuSO4溶液 正极反应为Cu-2e- = Cu2+ 在外电路中,电流从Cu极流向Ag极 将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同
2H2S + SO2 = 3S↓ + 2H2O (复分解反应) 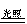 CO2 + 2CO (化合反应)
CO2 + 2CO (化合反应) 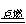 C.2AgBr 2Ag + Br2↑ (分解反应) 2Mg + CO2 2MgO +C. (置换反应)
C.2AgBr 2Ag + Br2↑ (分解反应) 2Mg + CO2 2MgO +C. (置换反应)
Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)ΔH.=+317.3kJ·mol-1 Zn+Ag2O===ZnO+2Ag ΔH.=+317.3kJ·mol-1 Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)ΔH.=-317.3kJ 2Zn(s)+2Ag2O(s)===2ZnO(s)+4Ag(s)ΔH.=-634.6 kJ·mol-1
2ag 3ag 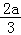 g 1.5ag
g 1.5ag
稀硫酸滴在银片上:2Ag+2H+=2Ag++H2↑ 铜片插入硝酸银溶液:Cu+Ag+=Cu2++Ag 氢氧化钠和醋酸反应:Na++OH- +CH3COO- +H+= CH3COONa+H2O 氧化铁与稀盐酸混合:Fe2O3+6H+=2Fe3++3H2O
M的金属活动性比Ag强 金属M可能是铜 该反应属于复分解反应 该反应前后M的化合价发生了改变

 2CO (化合反应) C. 2AgBr
2CO (化合反应) C. 2AgBr 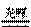 2Ag + Br2↑(分解反应) 2Mg + CO2
2Ag + Br2↑(分解反应) 2Mg + CO2  2MgO +C.(置换反应)
2MgO +C.(置换反应)
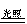 CO2 + 2CO (化合反应)
CO2 + 2CO (化合反应) 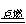 C.2AgBr 2Ag + Br2↑ (分解反应) 2Mg + CO2 2MgO +C. (置换反应)
C.2AgBr 2Ag + Br2↑ (分解反应) 2Mg + CO2 2MgO +C. (置换反应)
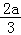 g 1.5ag
g 1.5ag