
 中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO
中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO 参与该反应,则转移的电子的物质的量为5 mol
参与该反应,则转移的电子的物质的量为5 mol
 中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO
中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO 参与该反应,则转移的电子的物质的量为5 mol
参与该反应,则转移的电子的物质的量为5 mol
 中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO
中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO 参与该反应,则转移的电子的物质的量为5 mol
参与该反应,则转移的电子的物质的量为5 mol
 中的R.只能被还原 元素R.位于周期表中第ⅤA.族 若1 mol RO
中的R.只能被还原 元素R.位于周期表中第ⅤA.族 若1 mol RO 参与该反应,则转移电子的物质的量为5 mol
参与该反应,则转移电子的物质的量为5 mol
 中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO
中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO 参与该反应,则转移的电子的物质的量为5 mol
参与该反应,则转移的电子的物质的量为5 mol
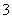 中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO
中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO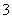 参与该反应,则转移的电子的物质的量为5 mol
参与该反应,则转移的电子的物质的量为5 mol
 中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO
中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO 参与该反应,则转移的电子的物质的量为5 mol
参与该反应,则转移的电子的物质的量为5 mol
 中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO
中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO 参与该反应,则转移的电子的物质的量为5 mol
参与该反应,则转移的电子的物质的量为5 mol
 中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO
中的R.只能被还原 R2在常温常压下一定是气体 若1 mol RO 参与该反应,则转移的电子的物质的量为5 mol
参与该反应,则转移的电子的物质的量为5 mol