你可能感兴趣的试题
+3B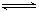 2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是 ( )A.u D.=0.4 mol / (L・s) u =0.5 mol / (L・s)C.u B.=0.6 mol / (L・s)
2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是 ( )A.u D.=0.4 mol / (L・s) u =0.5 mol / (L・s)C.u B.=0.6 mol / (L・s) 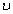 A=0.15 mol / (L・s)
A=0.15 mol / (L・s)
可逆反应达到平衡的重要特征是各物质的反应速率相等。 在可逆反应里,正反应的速率是正值,逆反应的速率是负值。 对于H2+I2  2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
(g)+3B(g) 2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大 的是 A.vA.=0.15mol/(L·min) v B.=0.6 mol/(L·min) v C.=0.3 mol/(L·min) v D.=0.1 mol/(L·min)
2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大 的是 A.vA.=0.15mol/(L·min) v B.=0.6 mol/(L·min) v C.=0.3 mol/(L·min) v D.=0.1 mol/(L·min)
在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,叫做可逆反应。 所有的化学反应都是可逆的 有气体参加的反应或有气体生成的反应,一定要在密闭体系的条件下才能是可逆反应 可逆反应中,正反应和逆反应是相对的
+2B 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( ) 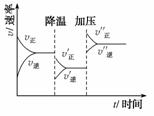 A.正反应是吸热反应 若A.B.是气体,则D.是液体或固体 逆反应是放热反应 A.B.C.D.均为气体
A.正反应是吸热反应 若A.B.是气体,则D.是液体或固体 逆反应是放热反应 A.B.C.D.均为气体
在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,叫可逆反应 所有的化学反应都是可逆的 有气体参加的反应或有气体生成的反应,一定要在密闭体系的条件下才能是可逆反应 可逆反应中,正反应和逆反应是相对的
(g)+3B(g) 2C.(g)+2D(g)在四种不同情况下反应速率分别如下,其中反应速率最大的是( ) A.vA.=0.15 mol/(L·min) vB.=0.6 mol/(L·min) vC.=0.3 mol/(L·min) vD.=0.1 mol/(L·min)
2C.(g)+2D(g)在四种不同情况下反应速率分别如下,其中反应速率最大的是( ) A.vA.=0.15 mol/(L·min) vB.=0.6 mol/(L·min) vC.=0.3 mol/(L·min) vD.=0.1 mol/(L·min)
+2B⇌2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断 ( ) A.正反应是吸热反应 若A.B.是气体,则D.是液体或固体 逆反应是放热反应 A.B.C.D.均为气体
不同的可逆反应,反应物的性质不同,平衡常数是相等的 对可逆反应来说,平衡常数越大,表示反应达到平衡时生成物浓度和反应物浓度的比值越大 对于同一个可逆反应,在不同的温度下,平衡常数有相同的数值 对可逆反应来说,平衡常数越大,表示反应完成的程度越小,物质的转化率越大
各物质的量保持不变 各物质的量继续改变 V(逆=V(正),正逆反应停止 N2 、H2、NH3的速率相等
(g)+ (g)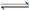 2C(g)+2D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( ) A. vA.=0.4 mol/(L·min) B. vB.=0.5 mol/(L·min) vC.=0.5 mol/(L·min) vD.=0.02 mol/(L·s)
2C(g)+2D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( ) A. vA.=0.4 mol/(L·min) B. vB.=0.5 mol/(L·min) vC.=0.5 mol/(L·min) vD.=0.02 mol/(L·s)
+3B 2C+2D(各物质均为气体),在不同情况下测得有下列4 种 反应速率,其中反应最快的是 A.vD.=0.4 mol / (L·s) v =0.5 mol / (L·s) C.vB.=0.6 mol / (L·s) vA.=0.15 mol / (L·s)
2C+2D(各物质均为气体),在不同情况下测得有下列4 种 反应速率,其中反应最快的是 A.vD.=0.4 mol / (L·s) v =0.5 mol / (L·s) C.vB.=0.6 mol / (L·s) vA.=0.15 mol / (L·s)
可逆反应达到平衡时,正反应的平衡常数等于逆反应的平衡常数 可逆反应达到平衡时,正反应速率等于逆反应速率 可逆反应达到平衡时,参与反应的各物质的浓度保持不变 可逆反应达到平衡时,产物浓度幂的乘积与反应物浓度幂的乘积之比,在一定温度下是常数
不同的可逆反应,反应物的性质不同,平衡常数是相同的 对可逆反应来说,平衡常数越大,表示反应达到平衡时生成物浓度和反应物浓度的比值越大 对于同一个可逆反应,在不同温度下,平衡常数有相同的数值 对于可逆反应来说,平衡常数越大,也就是反应完成的程度越小,物质的转化率越大
各物质的量保持不变 各物质的量继续改变 V(逆=V(正),正逆反应停止 N2 、H2、NH3的速率相等
+2B⇌2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断 ( ) A.正反应是吸热反应 若A.B.是气体,则D.是液体或固体 逆反应是放热反应 A.B.C.D.均为气体
+3B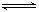 2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是 A.u( D.)=0.4 mol / (L.·s)
2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是 A.u( D.)=0.4 mol / (L.·s) 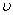 ( )=0.8mol / (L.·s) C.u( B.)=0.6 mol / (L.·s) u( A.)=0.5 mol / (L.·s)
( )=0.8mol / (L.·s) C.u( B.)=0.6 mol / (L.·s) u( A.)=0.5 mol / (L.·s)
vA.=0.45 mol·L-1·s-1 vB.=0.6 mol·L-1·s-1 vC.=0.5 mol·L-1·s-1 vD.=0.4 mol·L-1·s-1
不同的可逆反应,反应物的性质不同,平衡常数是相同的 对可逆反应来说,平衡常数越大,表示反应达到平衡时生成物浓度和反应物浓度的比值越大 对于同一个可逆反应,在不同温度下,平衡常数有相同的数值 对可逆反应来说,平衡常数越大,也就是反应完成的程度越小,物质的转化率越大

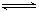 2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是 ( )A.u D.=0.4 mol / (L・s) u =0.5 mol / (L・s)C.u B.=0.6 mol / (L・s)
2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是 ( )A.u D.=0.4 mol / (L・s) u =0.5 mol / (L・s)C.u B.=0.6 mol / (L・s) 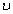 A=0.15 mol / (L・s)
A=0.15 mol / (L・s)
 2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
2HI,当有1mol H-H键断裂的同时,有2mol H-I键生成,说明此可逆反应已达到平衡。 在一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物和生成物的浓度不再发生变化,这就是该反应所达到的限度。
 2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大 的是 A.vA.=0.15mol/(L·min) v B.=0.6 mol/(L·min) v C.=0.3 mol/(L·min) v D.=0.1 mol/(L·min)
2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大 的是 A.vA.=0.15mol/(L·min) v B.=0.6 mol/(L·min) v C.=0.3 mol/(L·min) v D.=0.1 mol/(L·min)
 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )  A.正反应是吸热反应 若A.B.是气体,则D.是液体或固体 逆反应是放热反应 A.B.C.D.均为气体
A.正反应是吸热反应 若A.B.是气体,则D.是液体或固体 逆反应是放热反应 A.B.C.D.均为气体
 2C.(g)+2D(g)在四种不同情况下反应速率分别如下,其中反应速率最大的是( ) A.vA.=0.15 mol/(L·min) vB.=0.6 mol/(L·min) vC.=0.3 mol/(L·min) vD.=0.1 mol/(L·min)
2C.(g)+2D(g)在四种不同情况下反应速率分别如下,其中反应速率最大的是( ) A.vA.=0.15 mol/(L·min) vB.=0.6 mol/(L·min) vC.=0.3 mol/(L·min) vD.=0.1 mol/(L·min)
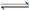 2C(g)+2D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( ) A. vA.=0.4 mol/(L·min) B. vB.=0.5 mol/(L·min) vC.=0.5 mol/(L·min) vD.=0.02 mol/(L·s)
2C(g)+2D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( ) A. vA.=0.4 mol/(L·min) B. vB.=0.5 mol/(L·min) vC.=0.5 mol/(L·min) vD.=0.02 mol/(L·s)
 2C+2D(各物质均为气体),在不同情况下测得有下列4 种 反应速率,其中反应最快的是 A.vD.=0.4 mol / (L·s) v =0.5 mol / (L·s) C.vB.=0.6 mol / (L·s) vA.=0.15 mol / (L·s)
2C+2D(各物质均为气体),在不同情况下测得有下列4 种 反应速率,其中反应最快的是 A.vD.=0.4 mol / (L·s) v =0.5 mol / (L·s) C.vB.=0.6 mol / (L·s) vA.=0.15 mol / (L·s)
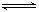 2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是 A.u( D.)=0.4 mol / (L.·s)
2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是 A.u( D.)=0.4 mol / (L.·s) 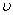 ( )=0.8mol / (L.·s) C.u( B.)=0.6 mol / (L.·s) u( A.)=0.5 mol / (L.·s)
( )=0.8mol / (L.·s) C.u( B.)=0.6 mol / (L.·s) u( A.)=0.5 mol / (L.·s)