你可能感兴趣的试题
平衡时,乙中CO2的转化率大于60% 平衡时,甲中和丙中H2的转化率均是60% 平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol/L 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
乙中SO3的平衡转化率为α1=20% 平衡时,丙中c(SO3)是甲中的2倍 平衡时,α3<α1 该温度下,平衡常数的值为400
Q1>Q3>Q2 =78.8kJ 三个容器中反应的平衡常数均为K=2 甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50% 若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)=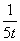 mol/(L.·min)
mol/(L.·min)
Q1 =Q32 达到平衡时,乙容器中SO2的体积分数最大 平衡时,甲、乙、丙3个容器中甲的平衡常数最小 若在上述条件下,反应生成1molSO3(s),则反应放热为98.5kJ
放出热量关系:a < b < 92.4 三个容器内反应的平衡常数:③ > ① > ② 平衡时氨气的体积分数:① > ③ N2的转化率:② > ① > ③
平衡时,乙中CO2的转化率大于60% 平衡时,甲中和丙中H2的转化率均是60% 平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol/L 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
甲中反应的平衡常数小于乙
该温度下,平衡常数值为400
平衡时,丙中c(SO3)是甲中的2倍
平衡时,甲中O2的转化率大于乙中O2的转化率
平衡时,乙中CO2的转化率大于60% 平衡时,甲中和丙中CO2的转化率均是60% 平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol/L 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
甲中达到平衡所需时间最短 平衡时,反应的平衡常数 平衡时,乙和丙中H2的转化率均是60% 平衡时,丙中c(CO)是甲中的2倍,是0.012mol/L
平衡时,乙和丙中H2的转化率均是60% 平衡时,丙中c(CO)是甲中的2倍,是0.012mol/L
平衡时,丙中SO2的转化率大于50% 当反应平衡时,乙中c(NO2)是甲中的2倍 温度升至90°C,上述反应平衡常数为25/16,则正反应为吸热反应 其他条件不变,若起始时向容器乙中充入0.10mol·L-1NO2和0.20mol·L-1SO2,达到平衡时c(NO)与原平衡相同
平衡时,乙中SO2的转化率大于50% 当反应平衡时,丙中c(SO2)是甲中的2倍 温度升至90℃,上述反应平衡常数为25/16,则正反应为吸热反应 其他条件不变,若起始时向容器乙中充入0.10mol ·L.-1 NO2和0.20 mol ·L.-1 SO2,达到平衡时c(NO)与原平衡不同
甲中反应的平衡常数小于乙 该温度下,平衡常数值为400 平衡时,丙中c(SO3)是甲中的2倍 平衡时,甲中O2的转化率大于乙中O2的转化率
(g)+3B(g)  2C(g),5 min后各容器反应达平衡状态,其中甲容器中A.的物质的量为0.4 mol。 反应前各物质的物质的量/mol A. C. 甲 1 3 0 乙 0 0 2 丙 1.5 4.5 1 下列说法正确的是 ( ) A.乙中5 min内 的反应速率为0.16 mol·L-1·min-1 B.达到平衡时,丙中A.的浓度是甲中的2倍 C.丙中反应的平衡常数大于甲中反应的平衡常数 达到平衡时,甲乙两容器中C.的物质的量百分含量相等
2C(g),5 min后各容器反应达平衡状态,其中甲容器中A.的物质的量为0.4 mol。 反应前各物质的物质的量/mol A. C. 甲 1 3 0 乙 0 0 2 丙 1.5 4.5 1 下列说法正确的是 ( ) A.乙中5 min内 的反应速率为0.16 mol·L-1·min-1 B.达到平衡时,丙中A.的浓度是甲中的2倍 C.丙中反应的平衡常数大于甲中反应的平衡常数 达到平衡时,甲乙两容器中C.的物质的量百分含量相等
平衡时,乙中CO2的转化率大于60% 平衡时,甲中和丙中H2的转化率均是60% 平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol·L.-1 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
容器乙中反应从开始到达平衡的反应速率为v(H2)=0.3mol·L-1·min-1 在该温度下甲容器中反应的平衡常数 2c1<1.5 2ρ1=ρ2
2c1<1.5 2ρ1=ρ2
该反应为吸热反应 容器Ⅲ达到平衡时,再充入少量氦气,平衡将向正反应方向移动 容器Ⅱ达到平衡时,容器中COS的物质的量浓度为0.025 mol • L-1 607K.时,该反应的平衡常数为0.50
Q1 =Q32 达到平衡时,乙容器中SO2的体积分数最大 平衡时,甲、乙、丙3个容器中甲的平衡常数最小 若在上述条件下,反应生成1molSO3(s),则反应放热为98.5kJ
平衡时,乙中CO2的转化率大于60% 平衡时,甲中和丙中H2的转化率均是60% 平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
平衡时,乙中H2的转化率是甲中的2倍 平衡时,甲中混合物的颜色比乙中深 平衡时,甲、乙中热量的变化值相等 该温度下,反应的平衡常数K=0.25
甲中反应的平衡常数小于乙 该温度下,平衡常数值为400 平衡时,丙中c(SO3)是甲中的2倍 平衡时,甲中O2的转化率大于乙中O2的转化率

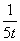 mol/(L.·min)
mol/(L.·min)
 平衡时,乙和丙中H2的转化率均是60% 平衡时,丙中c(CO)是甲中的2倍,是0.012mol/L
平衡时,乙和丙中H2的转化率均是60% 平衡时,丙中c(CO)是甲中的2倍,是0.012mol/L
 2C(g),5 min后各容器反应达平衡状态,其中甲容器中A.的物质的量为0.4 mol。 反应前各物质的物质的量/mol A. C. 甲 1 3 0 乙 0 0 2 丙 1.5 4.5 1 下列说法正确的是 ( ) A.乙中5 min内 的反应速率为0.16 mol·L-1·min-1 B.达到平衡时,丙中A.的浓度是甲中的2倍 C.丙中反应的平衡常数大于甲中反应的平衡常数 达到平衡时,甲乙两容器中C.的物质的量百分含量相等
2C(g),5 min后各容器反应达平衡状态,其中甲容器中A.的物质的量为0.4 mol。 反应前各物质的物质的量/mol A. C. 甲 1 3 0 乙 0 0 2 丙 1.5 4.5 1 下列说法正确的是 ( ) A.乙中5 min内 的反应速率为0.16 mol·L-1·min-1 B.达到平衡时,丙中A.的浓度是甲中的2倍 C.丙中反应的平衡常数大于甲中反应的平衡常数 达到平衡时,甲乙两容器中C.的物质的量百分含量相等
 2c1<1.5 2ρ1=ρ2
2c1<1.5 2ρ1=ρ2