
υ(C)=0.8 mol/(L•s) υ(D)=1 mol/(L•s)
 2AB3(g)的△H>0 图②可表示压强(P.)对反应2A(g)+2B(g)
2AB3(g)的△H>0 图②可表示压强(P.)对反应2A(g)+2B(g) 3C(g)+D(s)的影响 图③可表示向醋酸溶液通人氨气时,溶液导电性随氨气量的变化 根据图④,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5
3C(g)+D(s)的影响 图③可表示向醋酸溶液通人氨气时,溶液导电性随氨气量的变化 根据图④,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5
 2C(g),平衡后增大压强,A.的百分含量减小,则n≥2。 对于反应2A(g)
2C(g),平衡后增大压强,A.的百分含量减小,则n≥2。 对于反应2A(g) B.(g) △H.<0,若体系温度不再变化说明反应达到平衡状态。 对于反应2A(g)
B.(g) △H.<0,若体系温度不再变化说明反应达到平衡状态。 对于反应2A(g) B.(g),恒温,恒容条件下气体密度不再变化,说明反应达到平衡状态 对于反应2A(g)
B.(g),恒温,恒容条件下气体密度不再变化,说明反应达到平衡状态 对于反应2A(g) B.(g),若vA.正=2vB.逆,说明反应达到平衡状态
B.(g),若vA.正=2vB.逆,说明反应达到平衡状态
 CO2(g)+H2(g)”中的ΔH.大于0
CO2(g)+H2(g)”中的ΔH.大于0 2AB3(g)”的ΔH.小于0
2AB3(g)”的ΔH.小于0 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大

 3C(g)+5D(g) B.3A(g)+ B(g)
3C(g)+5D(g) B.3A(g)+ B(g)
 2C(g)+2D(g) 3A(g)+ B(g)
2C(g)+2D(g) 3A(g)+ B(g) 
 2C(g)+ D(g) A.(g)+ 3B(g)
2C(g)+ D(g) A.(g)+ 3B(g)
 2C(g)+2D(g)
2C(g)+2D(g)
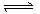 p (g)+q (g)经10 min后达到平衡,测得此时A.的浓度减少了n mol•L-1,C.的浓度增加了
p (g)+q (g)经10 min后达到平衡,测得此时A.的浓度减少了n mol•L-1,C.的浓度增加了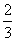 n mol•L-1,又知,平均反应速率vc=2vB 。达到平衡后,若保持温度不变,缩小容器体积,A.的转化率不变,那么该反应的化学方程式应为 A.2A(g)+6B(g)
n mol•L-1,又知,平均反应速率vc=2vB 。达到平衡后,若保持温度不变,缩小容器体积,A.的转化率不变,那么该反应的化学方程式应为 A.2A(g)+6B(g) 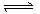 3C(g)+5D(g) B.3A(g)+B(g)
3C(g)+5D(g) B.3A(g)+B(g) 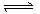 2C(g)+2D(g) C.3A(g)+B(g)
2C(g)+2D(g) C.3A(g)+B(g) 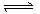 C.(g)+D(g) D.A.(g)+3B(g)
C.(g)+D(g) D.A.(g)+3B(g) 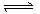 3C(g)+3D(g)
3C(g)+3D(g)