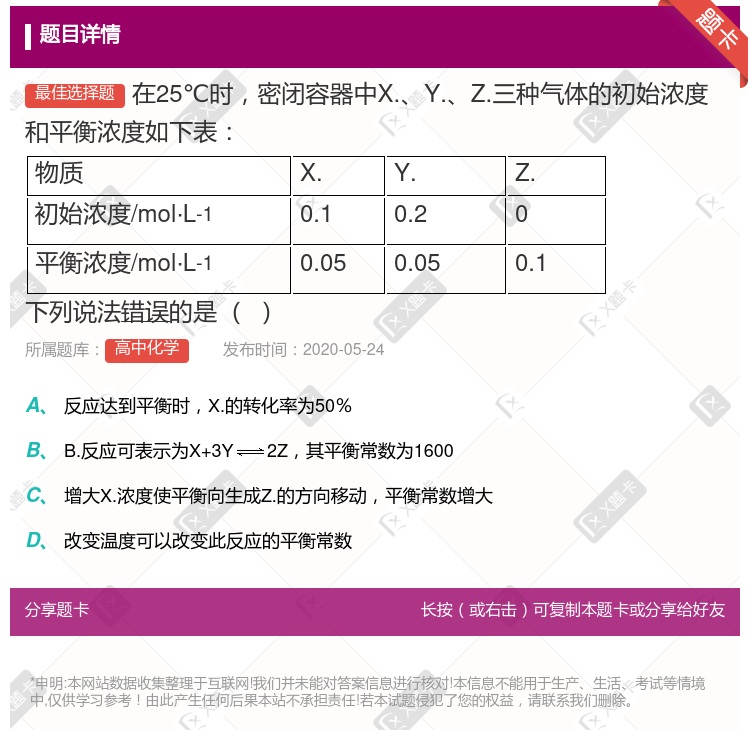
 2Z,其平衡常数为1600 (mol·L.-1)-2 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 (mol·L.-1)-2 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
 4Z+6W 反应达到平衡时,Y.的转化率为62.5% 加入催化剂其平衡常数不变,但使平衡向生成Z.的方向移动 改变温度可以改变此反应的平衡常数
4Z+6W 反应达到平衡时,Y.的转化率为62.5% 加入催化剂其平衡常数不变,但使平衡向生成Z.的方向移动 改变温度可以改变此反应的平衡常数
 2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
 2Z(g),其平衡常数为0.74 其它条件不变时,增大压强能使平衡向生成Z的方向移动,平衡常数也增大 改变温度可以改变此反应的平衡常数
2Z(g),其平衡常数为0.74 其它条件不变时,增大压强能使平衡向生成Z的方向移动,平衡常数也增大 改变温度可以改变此反应的平衡常数
 2Z,其平衡常数为1600 改变温度可以改变此反应的平衡常数 增大压强使平衡向生成Z.的方向移动,平衡常数增大
2Z,其平衡常数为1600 改变温度可以改变此反应的平衡常数 增大压强使平衡向生成Z.的方向移动,平衡常数增大
 2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
 2Z 若起始时X.、Y.、Z.的物质的量分别为0.1 mol、0.4mol、0.2 mol,达平衡时,Z.的体积分数一定增大 若起始时X.、Y.、Z.的物质的量分别为0.05 mol、0.15mol、0.1mol,达平衡时,X.的转化率一定与原投料相等。
2Z 若起始时X.、Y.、Z.的物质的量分别为0.1 mol、0.4mol、0.2 mol,达平衡时,Z.的体积分数一定增大 若起始时X.、Y.、Z.的物质的量分别为0.05 mol、0.15mol、0.1mol,达平衡时,X.的转化率一定与原投料相等。
 2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
 2Z,其平衡常数为1600 增大压强使平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 增大压强使平衡常数增大 改变温度可以改变此反应的平衡常数
 2Z,其平衡常数为1600 若该反应的正反应方向为放热反应,升高温度,化学反应速率增大,反应的平衡常数也增大
2Z,其平衡常数为1600 若该反应的正反应方向为放热反应,升高温度,化学反应速率增大,反应的平衡常数也增大
 2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
 2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
 2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
 2Z,其平衡常数为1 600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1 600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
 2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
 2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
 2Z,其平衡常数为1600 (mol·L-1)-2 增大压强使平衡向生成Z.的方向移动,平衡常数不变 改变温度或向平衡体系中加入X.都会使平衡移动,平衡常数也会随之改变
2Z,其平衡常数为1600 (mol·L-1)-2 增大压强使平衡向生成Z.的方向移动,平衡常数不变 改变温度或向平衡体系中加入X.都会使平衡移动,平衡常数也会随之改变
 2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数不变 若改变温度反应的平衡常数变大,则一定为升高温度
2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数不变 若改变温度反应的平衡常数变大,则一定为升高温度
 2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数
2Z,其平衡常数为1600 增大压强使平衡向生成Z.的方向移动,平衡常数增大 改变温度可以改变此反应的平衡常数 