你可能感兴趣的试题
C.2H6(g) +  O2(g)=2CO2(g) +3H2O(l) △H =-1560kJ·mol-1 2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(g) △H =-1560kJ·mol-1 2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(l) △H =+3120 kJ·mol-1 C.2H6(g) +
O2(g)=2CO2(g) +3H2O(l) △H =-1560kJ·mol-1 2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(g) △H =-1560kJ·mol-1 2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(l) △H =+3120 kJ·mol-1 C.2H6(g) + O2(g)=2CO2(g) +3H2O(l) △H =-52.0kJ·mol-1
O2(g)=2CO2(g) +3H2O(l) △H =-52.0kJ·mol-1
CuSO4发生了氧化反应 生成1molH.3PO4时,有10mol电子转移 氧化产物和还原产物的物质的量之比为6 : 5 白磷只作还原剂
42.59% 41.20% 21.29% 20.60%
鸟粪石既属于镁盐又属于磷酸盐 鸟粪石既能和强酸反应又能和强碱反应 鸟粪石中既含有离子键又含有共价键 鸟粪石中两种阳离子的电子式分别为 、
、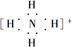
Na3PO4·1/4NaOCl·12H2O Na3PO4·1/4NaOCl·10H2O Na3PO4·1/4NaOCl·8H2O Na3PO4·1/4NaOCl·6H2O Na3PO4·1/4NaOCl·4H2O
MgNH4PO4-Mg2P2O2 Fe(OH)3-Fe2O3 Al(C9H6NO)3-Al(C9H6NO)3 CuR2-CuO(R代表铜铁灵)
用惰性电极电解NaH2PO2溶液,其阳极反应式为2H2O+4e- O.2↑+4H+ 将H.3PO2溶液加入到酸性高锰酸钾溶液中,H.3PO2的还原产物可能为H.3PO4 H.3PO2溶于水的电离方程式为H.3PO2
O.2↑+4H+ 将H.3PO2溶液加入到酸性高锰酸钾溶液中,H.3PO2的还原产物可能为H.3PO4 H.3PO2溶于水的电离方程式为H.3PO2 H.++H2PO2- H.3PO2与过量NaOH溶液反应的离子方程式为H.3PO2+3OH-
H.++H2PO2- H.3PO2与过量NaOH溶液反应的离子方程式为H.3PO2+3OH- PO23-+3H2O.
PO23-+3H2O.
沉淀形式是MgNH4PO4·6H2O,称量形式是Mg2P2O7 沉淀形式和称量形式都是MgNH4PO4·6H2O 沉淀形式和称量形式都是Mg2P2O7 沉淀形式是Mg2P2O7,称量形式是MgNH4PO4·6H2O
称量形式 组合稳定的化合物 大分子量化合物 化学性质稳定化合物 沉淀反应的最终产物
C6H12O6 → 2C3H4O3(丙酮酸)+4[H]+能量 2H2O → 4[H]+O2 2C3H4O3(丙酮酸)+6H2O → 6CO2+20[H]+能量 6CO2+12H2O → C6H12O6+6H2O+6O2
13.73% 14.20% 27.46% 28.39%
 O2(g)=2CO2(g) +3H2O(l) △H =-1560kJ·mol-1 2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(g) △H =-1560kJ·mol-1 2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(l) △H =+3120 kJ·mol-1 C.2H6(g) +
O2(g)=2CO2(g) +3H2O(l) △H =-1560kJ·mol-1 2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(g) △H =-1560kJ·mol-1 2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(l) △H =+3120 kJ·mol-1 C.2H6(g) + O2(g)=2CO2(g) +3H2O(l) △H =-52.0kJ·mol-1
O2(g)=2CO2(g) +3H2O(l) △H =-52.0kJ·mol-1
 、
、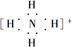
 O.2↑+4H+ 将H.3PO2溶液加入到酸性高锰酸钾溶液中,H.3PO2的还原产物可能为H.3PO4 H.3PO2溶于水的电离方程式为H.3PO2
O.2↑+4H+ 将H.3PO2溶液加入到酸性高锰酸钾溶液中,H.3PO2的还原产物可能为H.3PO4 H.3PO2溶于水的电离方程式为H.3PO2 H.++H2PO2- H.3PO2与过量NaOH溶液反应的离子方程式为H.3PO2+3OH-
H.++H2PO2- H.3PO2与过量NaOH溶液反应的离子方程式为H.3PO2+3OH- PO23-+3H2O.
PO23-+3H2O.