你可能感兴趣的试题
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l); ΔH.=-2b kJ • mol-1 C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l); ΔH.=2b kJ • mol-1 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l); ΔH.=-4b kJ • mol-1 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l); ΔH.=b kJ • mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH.=-2b kJ / mol 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH.=b kJ / mol C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l) ΔH.=2b kJ / mol 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH.=-4b kJ / mol
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH = - b KJ/mol C2H2(g)+5/2 O2(g)===2CO2(g)+ H2O(l) ΔH = +2b KJ/mol 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH = -4b KJ/mol C2H2(g)+ O2(g)=== CO2(g)+ H2O(l) ΔH = + b KJ/mol
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2bkJ/mol C2H2(g)+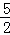 O2(g)═2CO2(g)+H2O(l)△H=+2bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+bkJ/mol
O2(g)═2CO2(g)+H2O(l)△H=+2bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+bkJ/mol
2C2H2(g) + 5O2(g) = 4CO2(g) + 2H2O(l) ΔH = -2b kJ / mol C2H2(g) + 5/2O2(g) = 2CO2(g) + H2O(l) ΔH = -b kJ / mol 2C2H2(g) + 5O2(g) = 4CO2(g) + 2H2O(l) ΔH - -4b kJ / mol C2H2(g) + 5/2O2(g) = 2CO2(g) + H2O(g) ΔH - b kJ / mol
2C2H2(g) + 5O2(g) = 4CO2(g) + 2H2O(l) △H=-4b kJ/mol C2H2(g) + 5/2O2(g) = 2CO2(g) + H2O(l) △H=2b kJ/mol 2C2H2(g) + 5O2(g) = 4CO2(g) + 2H2O(l) △H=-2b kJ/mol 2C2H2(g) + 5O2(g) = 4CO2(g) + 2H2O(l) △H=b kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(1); △H.=-4b kJ/mol C2H2(g)+2.5O2(g)=2CO2(g)+H2O(1); △H.=2b kJ/mol 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(1); △H.=―2b kJ/mol 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(1); △H.=b kJ/mol
充分燃烧ag乙炔气体时生成1mol二氧化碳气体和液态水,可放出b kJ热量,则乙炔燃烧的热化学方程式为:2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-4bkJ・mol―1 已知 (s)+ O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJC.反应热的大小与反应物所具有的能量和生成物所具有的能量无关,而只与化反应体系的始态和终点状态有关 0.5mol的稀硫酸与0.5mol氢氧化钡稀溶液生成1mol水反应的得到反应热就是中和热
O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJC.反应热的大小与反应物所具有的能量和生成物所具有的能量无关,而只与化反应体系的始态和终点状态有关 0.5mol的稀硫酸与0.5mol氢氧化钡稀溶液生成1mol水反应的得到反应热就是中和热
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2b kJ·mol﹣1 C2H2(g)+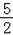 O2(g)═2CO2(g)+H2O(l)△H=+2b kJ·mol﹣1 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4b kJ·mol﹣1 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+b kJ·mol﹣1
O2(g)═2CO2(g)+H2O(l)△H=+2b kJ·mol﹣1 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4b kJ·mol﹣1 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+b kJ·mol﹣1
2C2H2(g)+5O2(g)====4CO2(g)+2H2O(l) ΔH=-4b kJ·mol-1 C2H2(g)+ O2(g)====2CO2(g)+H2O(l) ΔH=2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=-2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=b kJ·mol-1
O2(g)====2CO2(g)+H2O(l) ΔH=2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=-2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=b kJ·mol-1
2C2H2(g) + 502(g) = 4C02 (g) + 2H20 (1) △H= -2b kJ.mol-l C2H2(g) +  02(g) = 2C02 (g) + H20 (1) △H= 2b kJ.mol-l 2C2H2(g) + 502(g) = 4C02 (g) + 2H20 (1) △H= -4b kJ.mol-l 2C2H2(g) + 502(g) = 4C02 (g) + 2H20 (1) △H= b kJ.mol-l
02(g) = 2C02 (g) + H20 (1) △H= 2b kJ.mol-l 2C2H2(g) + 502(g) = 4C02 (g) + 2H20 (1) △H= -4b kJ.mol-l 2C2H2(g) + 502(g) = 4C02 (g) + 2H20 (1) △H= b kJ.mol-l
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-4bkJ・mol-1
C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l)ΔH=2bkJ・mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=-2bkJ・mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)ΔH=bkJ・mol-1
2C2H2(g)+5O2(g)====4CO2(g)+2H2O(l) ΔH=-4b kJ·mol-1 C2H2(g)+ O2(g)====2CO2(g)+H2O(l) ΔH=2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=-2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=b kJ·mol-1
O2(g)====2CO2(g)+H2O(l) ΔH=2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=-2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=b kJ·mol-1
2C2H2(g) + 5O2(g) == 4CO2(g) + 2H2O(l);△H = -2b KJ/mol C2H2(g) + 5/2O2(g) == 2CO2(g) + H2O(l);△H=2bKJ/mol 2C2H2(g) + 5O2(g) == 4CO2(g) + 2H2O(l);△H = b KJ/mol 2C2H2(g) + 5O2(g) == 4CO2(g) + 2H2O(l);△H = -4b KJ/mol
2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l)△H=-4b kJ/mol C2H2(g)+ O2(g)
O2(g) 2CO2(g)+H2O(l) △H= -b kJ/mol 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l)△H=-2b kJ/mol 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l)△H= +4b kJ/mol
参加反应的乙炔和氧气的化学计量数之比为2:5 参加反应的乙炔和生成的二氧化碳的分子个数比为1:2 参加反应的乙炔和氧气的质量比为2:5 参加反应的乙炔和生成的二氧化碳的体积比为1:2
2C2H2(g) + 5O2(g)= 4CO2(g) + 2H2O(l)△H.= -4b KJ/mol C2H2(g) + 5/2O2(g)= 2CO2(g) + H2O(l)△H.= 2b KJ/mol 2C2H2(g)+ 5O2(g)=4CO2(g) + 2H2O(l)△H.= -2b KJ/mol 2C2H2(g) + 5O2(g)= 4CO2(g) + 2H2O(l)△H.= b KJ/mol
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2bkJ/mol C2H2(g)+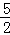 O2(g)═2CO2(g)+H2O(l)△H=+2bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+bkJ/mol
O2(g)═2CO2(g)+H2O(l)△H=+2bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+bkJ/mol
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-2b kJ·mol-1 C2H2(g)+ O2(g)===2CO2(g)+H2O(l) ΔH.=+2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-4b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=+b kJ·mol-1
O2(g)===2CO2(g)+H2O(l) ΔH.=+2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-4b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=+b kJ·mol-1
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-4b kJ·mol-1 C2H2(g)+ O2(g)===2CO2(g)+H2O(l) ΔH.=2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-b kJ·mol-1
O2(g)===2CO2(g)+H2O(l) ΔH.=2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-b kJ·mol-1

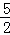 O2(g)═2CO2(g)+H2O(l)△H=+2bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+bkJ/mol
O2(g)═2CO2(g)+H2O(l)△H=+2bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+bkJ/mol
 O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJC.反应热的大小与反应物所具有的能量和生成物所具有的能量无关,而只与化反应体系的始态和终点状态有关 0.5mol的稀硫酸与0.5mol氢氧化钡稀溶液生成1mol水反应的得到反应热就是中和热
O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJC.反应热的大小与反应物所具有的能量和生成物所具有的能量无关,而只与化反应体系的始态和终点状态有关 0.5mol的稀硫酸与0.5mol氢氧化钡稀溶液生成1mol水反应的得到反应热就是中和热
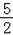 O2(g)═2CO2(g)+H2O(l)△H=+2b kJ·mol﹣1 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4b kJ·mol﹣1 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+b kJ·mol﹣1
O2(g)═2CO2(g)+H2O(l)△H=+2b kJ·mol﹣1 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4b kJ·mol﹣1 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+b kJ·mol﹣1
 O2(g)====2CO2(g)+H2O(l) ΔH=2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=-2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=b kJ·mol-1
O2(g)====2CO2(g)+H2O(l) ΔH=2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=-2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=b kJ·mol-1
 02(g) = 2C02 (g) + H20 (1) △H= 2b kJ.mol-l 2C2H2(g) + 502(g) = 4C02 (g) + 2H20 (1) △H= -4b kJ.mol-l 2C2H2(g) + 502(g) = 4C02 (g) + 2H20 (1) △H= b kJ.mol-l
02(g) = 2C02 (g) + H20 (1) △H= 2b kJ.mol-l 2C2H2(g) + 502(g) = 4C02 (g) + 2H20 (1) △H= -4b kJ.mol-l 2C2H2(g) + 502(g) = 4C02 (g) + 2H20 (1) △H= b kJ.mol-l
 O2(g)====2CO2(g)+H2O(l) ΔH=2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=-2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=b kJ·mol-1
O2(g)====2CO2(g)+H2O(l) ΔH=2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=-2b kJ·mol-1 2C2H2(g)+5O2(g) ====4CO2(g)+2H2O(l) ΔH=b kJ·mol-1
 O2(g)
O2(g)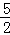 O2(g)═2CO2(g)+H2O(l)△H=+2bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+bkJ/mol
O2(g)═2CO2(g)+H2O(l)△H=+2bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4bkJ/mol 2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=+bkJ/mol
 O2(g)===2CO2(g)+H2O(l) ΔH.=+2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-4b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=+b kJ·mol-1
O2(g)===2CO2(g)+H2O(l) ΔH.=+2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-4b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=+b kJ·mol-1
 O2(g)===2CO2(g)+H2O(l) ΔH.=2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-b kJ·mol-1
O2(g)===2CO2(g)+H2O(l) ΔH.=2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-2b kJ·mol-1 2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH.=-b kJ·mol-1