你可能感兴趣的试题
氢气和氯气反应生成氯化氢气体的热化学方程式为:H2(g)+Cl2(g)=2HCl(g) 氢气和氯气反应生成2mol氯化氢气体,反应的△H.=183kJ·mol-1 氢气和氯气反应生成2mol氯化氢气体,反应的△H.=-183kJ·mol-1 氢气和氯气反应生成1mol氯化氢气体,反应的△H.=-183kJ·mol-1
氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g) 2HCl(g) 氢气和氯气反应生成2mol氯化氢气体,反应的△H=183kJ/mol 氢气和氯气反应生成2mol氯化氢气体,反应的△H=-183kJ/mol 氢气和氯气反应生成1mol氯化氢气体,反应的△H=-183kJ/mol
2HCl(g) 氢气和氯气反应生成2mol氯化氢气体,反应的△H=183kJ/mol 氢气和氯气反应生成2mol氯化氢气体,反应的△H=-183kJ/mol 氢气和氯气反应生成1mol氯化氢气体,反应的△H=-183kJ/mol
氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl(g)=2HCl(g) 氢气与氯气反应生成2mol氯化氢气体,反应的△H.=183kJ/mol 氢气与氯气反应生成2mol氯化氢气体,反应的△H.=—183kJ/mol 氢气与氯气反应生成1mol氯化氢气体,反应的△H.=—183kJ/mol
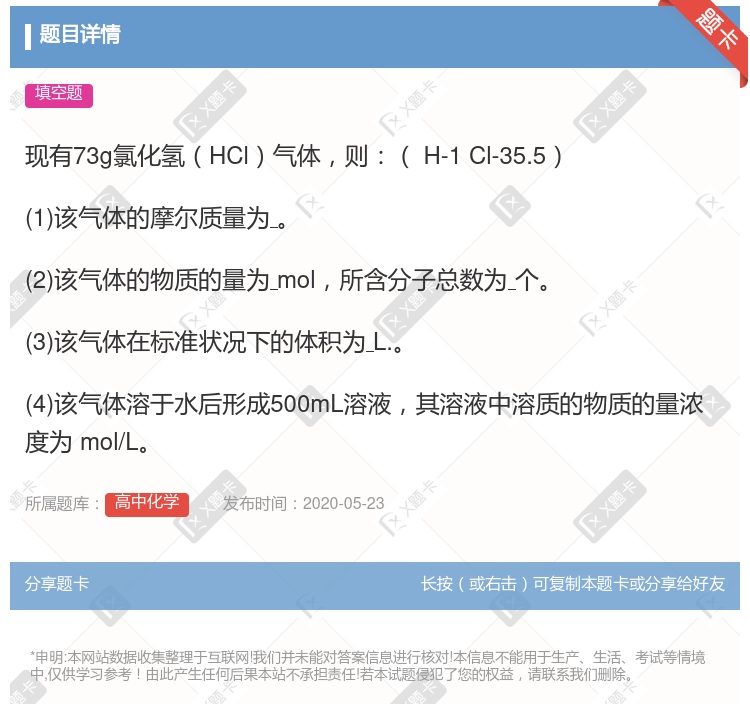
装置③可用于收集H2、CO2、Cl2、NH3等气体 装置②可用于吸收NH3或HCl气体,并防止倒吸 装置①常用于分离互不相溶的液体混合物 装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢
氢气和氯气反应生成氯化氢气体的热化学方程式是 H2 (g) + Cl2 (g) == 2HCl(g) 氢气和氯气反应生成 2 mol 氯化氢气体,反应的D.H. == +183 kJ·mol-1 氢气和氯气反应生成 1 mol 氯化氢气体,反应的 H. == -183 kJ·mol-1 D.氢气和氯气反应生成 2 mol 氯化氢气体,反应的D.H. == -183 kJ·mol-1
氢气与氯气反应生成1 mol氯化氢气体,反应吸收248 kJ的能量 436 kJ·mol-1是指断开1 mol H2中的H.-H.键需要放出436 kJ的能量 氢气与氯气反应生成2 mol氯化氢气体,反应放出183 kJ的能量 431 kJ·mol-1是指生成2 mol HCl中的H.—Cl键需要放出431 kJ的能量
氢气和氯气反应生成氯化氢气体的热化学方程式是 H2(g)+Cl2(g)=2HCl(g) 氢气和氯气反应生成2mol氯化氢气体,反应的△H=183kJ/mol 氢气和氯气反应生成2mol氯化氢气体,反应的△H=-183kJ/mol 氢气和氯气反应生成1mol氯化氢气体,反应的△H=-183kJ/mol
氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)=2HCl(g) 氢气和氯气反应生成2mol氯化氢气体,反应的△H=183kJ/mol 氢气和氯气反应生成2mol氯化氢气体,反应的△H=-183kJ/mol 氢气和氯气反应生成1mol氯化氢气体,反应的△H=-183kJ/mol
氢气和氯气反应生成氯化氢气体的热化学方程式是 H2(g)+Cl2(g)=2HCl(g)
氢气和氯气反应生成 2mol 氯化氢气体,反应的△H=183kJ/mol
氢气和氯气反应生成 2mol 氯化氢气体,反应的△H=﹣183kJ/mol
氢气和氯气反应生成 1mol 氯化氢气体,反应的△H=﹣183kJ/mol
氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)=2HCl(g)
氢气和氯气反应生成2 mol氯化氢气体,反应的△H=+183kJ/mol
氢气和氯气反应生成1 mol氯化氢气体,反应的△H=-183kJ/mol
氢气和氯气反应生成2mol氯化氢气体,反应的△H=-183kJ/mol
氢气和氯气反应生成氯化氢气体的热化学方程式是: H2( g)+Cl2(g)=2HCl(g) 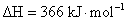 氢气和氯气反应生成2 mol氯化氢气体,反应的
氢气和氯气反应生成2 mol氯化氢气体,反应的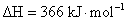 氢气和氯气反应生成2mol氯化氢气体,反应的
氢气和氯气反应生成2mol氯化氢气体,反应的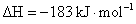 氢气和氯气反应生成1 mol氯化氢气气体,反应的
氢气和氯气反应生成1 mol氯化氢气气体,反应的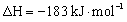
氢气和氯气反应生成氯化氢气体的热化学反应式是H2(g)+Cl2 (g)=2HCl(g) 氢气与氯气反应生成2molHCl气体,反应的ΔH=183kJ/mol 氢气与氯气反应生成2molHCl气体,反应的ΔH=-183kJ/mol 氢气与氯气生成氯化氢的反应是放热反应,在常温常压下就能自发进行
氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)=2HCl(g) 氢气和氯气反应生成2 mol氯化氢气体,反应的△H.=183kJ/mol 氢气和氯气反应生成2 mol氯化氢气体,反应的△H.=-183kJ/mol 氢气和氯气反应生成1 mol氯化氢气体,反应的△H.=-183kJ/mol
氢气与氯气反应生成1 mol氯化氢气体,反应吸收248 kJ的能量 436 kJ/ mol是指断开1 mol H2中的H.—H.键需要放出436 kJ的能量 氢气与氯气反应生成2 mol氯化氢气体,反应放出183 kJ的能量 431 kJ/ mol是指生成2 mol HCl中的H.—Cl键需要放出431 kJ的能量
氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)===2HCl(g) 氢气和氯气反应生成2 mol氯化氢气体,反应的ΔH.=+183 kJ·mol-1 氢气和氯气反应生成2 mol氯化氢气体,反应的ΔH.=-183 kJ·mol-1 氢气和氯气反应生成1 mol氯化氢气体,反应的ΔH.=-183 kJ·mol-1
所有化学反应在反应前后分子个数都不发生变化 此反应过程中只有物质变化,没有能量变化 在任何条件下,H2和Cl2均不能大量共存 由微观示意图可知:2g H2和71g Cl2发生反应可生成73g HCl
 2HCl(g) 氢气和氯气反应生成2mol氯化氢气体,反应的△H=183kJ/mol 氢气和氯气反应生成2mol氯化氢气体,反应的△H=-183kJ/mol 氢气和氯气反应生成1mol氯化氢气体,反应的△H=-183kJ/mol
2HCl(g) 氢气和氯气反应生成2mol氯化氢气体,反应的△H=183kJ/mol 氢气和氯气反应生成2mol氯化氢气体,反应的△H=-183kJ/mol 氢气和氯气反应生成1mol氯化氢气体,反应的△H=-183kJ/mol
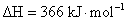 氢气和氯气反应生成2 mol氯化氢气体,反应的
氢气和氯气反应生成2 mol氯化氢气体,反应的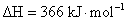 氢气和氯气反应生成2mol氯化氢气体,反应的
氢气和氯气反应生成2mol氯化氢气体,反应的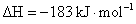 氢气和氯气反应生成1 mol氯化氢气气体,反应的
氢气和氯气反应生成1 mol氯化氢气气体,反应的