你可能感兴趣的试题
硫酸的摩尔质量是98 g 18 g水的物质的量为1 mol O2的摩尔质量(单位是g·mol-1)在数值上等于其相对分子质量 1 mol CO的质量为28 g·mol-1
该硫酸的物质的量浓度为9.2 mol/L. 该硫酸与等体积的水混合后,所得溶液的质量分数为49% 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL 该硫酸与等质量的水混合所得溶液的物质的量浓度等于9.2 mol/L
溶质物质的量浓度大于9.2mol/L 溶液体积为20mL 溶质质量分数为49% 溶质质量分数小于49%
a=10,b=9.2 a<10,b>9.2 a>10,b<9.2 a>10,b=9.2
0.5mol/L 0.1mol/L 0.5g/ml 1mol/L
9.2mol/L 大于9.2mol/L 小于9.2mol/L 不能确定
将w g a%的NaCl溶液蒸发掉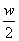 g水,得到2a%的NaCl溶液 将1体积c mol/L的硫酸用水稀释为5体积,稀溶液的物质的量浓度为0.2c mol/L 将5.85 g NaCl晶体溶于水配成1L溶液,制得0.01 mol/L的NaCl溶液 1 mol·L-1 AlCl3溶液中Cl-的物质的量浓度与3 mol·L-1 NH4Cl溶液中 Cl-的物质的量浓度相等
g水,得到2a%的NaCl溶液 将1体积c mol/L的硫酸用水稀释为5体积,稀溶液的物质的量浓度为0.2c mol/L 将5.85 g NaCl晶体溶于水配成1L溶液,制得0.01 mol/L的NaCl溶液 1 mol·L-1 AlCl3溶液中Cl-的物质的量浓度与3 mol·L-1 NH4Cl溶液中 Cl-的物质的量浓度相等
0.5mol/L 0.1mol/L 0.5g/mL 1mol/L
0.5mol/L 0.1mol/L 0.5g/mL 1mol/L
水的摩尔质量为18 g 水的摩尔质量为18 g·mol-1 1mol水的质量为18 g·mol-1 9g水的物质的量为1 mol
等体积硫酸铁、硫酸铜、硫酸钾溶液分别与足量的氯化钡溶液反应,若生成的硫酸钡沉淀的质量比为1∶2∶3,则三种硫酸盐溶液的物质的量浓度比为1∶2∶3 150 mL 1 mol·L-1的氯化钾溶液中的c(Cl-)与50 mL 1 mol·L-1的氯化铝溶液中的c(Cl-)相等 20℃时,饱和KCl溶液的密度为1.174 g·cm-3,物质的量浓度为4.0 mol·L-1,则此溶液中KCl的质量分数为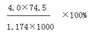 20℃时,100 g水可溶解34.2 g KCl,此时KCl饱和溶液的质量分数为34.2%
20℃时,100 g水可溶解34.2 g KCl,此时KCl饱和溶液的质量分数为34.2%
a>10,b<9.2 a<10,b>9.2 a=10,b=9.2 a>10,b=9.2
a>10,b<9.2 a<10,b>9.2 a=10,b=9.2 a>10,b=9.2
1L硫酸溶液中含98gH2SO4,则该溶液的物质的量浓度为98g/L 1L水溶解了0.5molNaCl,则该溶液的物质的量浓度为0.5mol/L 1000mLC12H22O11(蔗糖)溶液里含1mol C12H22O11,则该溶液的物质的量浓度为0.001mol/L 10mL 1mol/L的硫酸溶液与100mL 1mol/L的硫酸溶液的浓度相同。
a>10 b<9.2 a<10 b<9.2 a=10 b<9.2 a>10 b>9.2

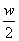 g水,得到2a%的NaCl溶液 将1体积c mol/L的硫酸用水稀释为5体积,稀溶液的物质的量浓度为0.2c mol/L 将5.85 g NaCl晶体溶于水配成1L溶液,制得0.01 mol/L的NaCl溶液 1 mol·L-1 AlCl3溶液中Cl-的物质的量浓度与3 mol·L-1 NH4Cl溶液中 Cl-的物质的量浓度相等
g水,得到2a%的NaCl溶液 将1体积c mol/L的硫酸用水稀释为5体积,稀溶液的物质的量浓度为0.2c mol/L 将5.85 g NaCl晶体溶于水配成1L溶液,制得0.01 mol/L的NaCl溶液 1 mol·L-1 AlCl3溶液中Cl-的物质的量浓度与3 mol·L-1 NH4Cl溶液中 Cl-的物质的量浓度相等
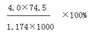 20℃时,100 g水可溶解34.2 g KCl,此时KCl饱和溶液的质量分数为34.2%
20℃时,100 g水可溶解34.2 g KCl,此时KCl饱和溶液的质量分数为34.2%