
 =0.1 mol/L的溶液:Na+, K+ , CO32-, NO3-
=0.1 mol/L的溶液:Na+, K+ , CO32-, NO3-
 含有大量
含有大量 的溶液:
的溶液: 加入铝粉能产生氢气的溶液:
加入铝粉能产生氢气的溶液: 由水电离出的
由水电离出的 溶液:
溶液:
 甲基橙呈红色的溶液:
甲基橙呈红色的溶液: pH=12的溶液:K+、Na+、CH3COO-、Br- 与铝反应产生大量氢气的溶液:
pH=12的溶液:K+、Na+、CH3COO-、Br- 与铝反应产生大量氢气的溶液:
 常温下的溶液:
常温下的溶液: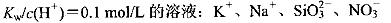 O.1 mol/L AgNO3溶液:
O.1 mol/L AgNO3溶液: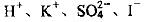 加入苯酚显紫色的溶液:
加入苯酚显紫色的溶液: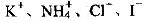
 甲基橙呈红色的溶液:NH
甲基橙呈红色的溶液:NH 、Ba2+、AlO
、Ba2+、AlO 、Cl- 与铝反应产生大量氢气的溶液:Na+、K.+、CO
、Cl- 与铝反应产生大量氢气的溶液:Na+、K.+、CO 、Cl- pH=12的溶液:K.+、Na+、CH3COO-、Br-
、Cl- pH=12的溶液:K.+、Na+、CH3COO-、Br-
 常温下的溶液:
常温下的溶液: O.1 mol/L AgNO3溶液:
O.1 mol/L AgNO3溶液: 加入苯酚显紫色的溶液:
加入苯酚显紫色的溶液: