你可能感兴趣的试题
a=4 将Y.均匀分散到水中形成的体系具有丁达尔效应 每有3 mol Fe2+ 参加反应,反应中转移的电子总数为5 mol S2O32-是还原剂
x=2 参加反应的Fe2+全部做还原剂 每生成1mol Fe3O4,反应转移的电子总数为4mol 1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol
FeO:Fe3O4:Fe2O3=95:4:1 FeO:Fe3O4:Fe2O3=50:45:5 FeO:Fe3O4:Fe2O3=5:45:50 FeO:Fe3O4:Fe2O3=1:4:95
每生成1 mol Fe3O4转移4 mol电子 该反应中Fe2+和S2O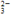 都是还原剂 3 mol Fe2+被氧化时有1 mol O2被还原 离子方程式中x=4
都是还原剂 3 mol Fe2+被氧化时有1 mol O2被还原 离子方程式中x=4
O2和S2O32-是氧化剂,Fe2+ 是还原剂 每生成1 mol Fe3O4,转移2 mol电子 若有2 mol Fe2+被氧化,则被Fe2+还原的O2为0.5 mol 参加反应的氧化剂与还原剂的物质的量之比为1∶5
每转移1.5 mol电子,有1.125 mol Fe2+被氧化 x=2 Fe2+、S2O 都是还原剂 每生成1 mol Fe3O4,反应中转移电子2 mol
都是还原剂 每生成1 mol Fe3O4,反应中转移电子2 mol
在反应中硫元素被氧化,铁元素被还原 还原剂是Fe2+,氧化剂是S2O32-和O2 每生成1mol Fe3O4,转移3mol电子 当转移1mol电子时,消耗56g S2O32-
每转移3mol电子,有1.5mol Fe2+被氧化 M.为OH—离子,x=2 O2、S2O32—都是氧化剂 每生成1molFe3O4,反应中转移2mol电子
Fe2+、S2O32-都是还原剂 每生成1 mol Fe3O4,则转移电子数为3 mol 硫元素被氧化,铁元素被还原 x=2
S2O32-是还原剂 Y.的化学式为Fe2O3 a =4 每有1molO2参加反应,转移的电子总数为4mol
将纳米Fe3O4分散在水中没有丁达尔现象 将纳米Fe3O4分散在水中Fe3O4不能透过滤纸 每生成1 mol Fe3O4反应转移的电子数为4 mol 反应物OH-的化学计量数x=2
M为OH-离子,x=2 每转移3 mol电子,有1.5 molFe2+被氧化 O2、S2O32-都是氧化剂 每生成1 mol Fe3O4,反应中转移2mol电子
硫元素被氧化,铁元素被还原 Fe2+、S2O32-都是还原剂 x=2 每生成1 mol Fe3O4,则转移电子数为3 mol
Fe2+是还原剂,S2O32—和O2是氧化剂 每生成1 mol Fe3O4反应转移的电子数为2 mol 若有2mol Fe2+被氧化,被Fe2+还原的O2为0.5mol 将纳米Fe3O4分散在水中Fe3O4不能透过滤纸

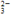 都是还原剂 3 mol Fe2+被氧化时有1 mol O2被还原 离子方程式中x=4
都是还原剂 3 mol Fe2+被氧化时有1 mol O2被还原 离子方程式中x=4
 都是还原剂 每生成1 mol Fe3O4,反应中转移电子2 mol
都是还原剂 每生成1 mol Fe3O4,反应中转移电子2 mol