你可能感兴趣的试题
向上述体系中加入CCl4,平衡不移动 25 C时,向上述体系中加入少量I2,平衡向右移动, 平衡常数大于680 该反应的平衡常数表达式为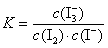 该反应的正反应为放热反应
该反应的正反应为放热反应
上述正反应为放热反应 上述体系中加入苯,平衡不移动 可运用该反应原理除去硫粉中少量的碘单质 实验室配制碘水时,为增大碘单质的溶解度可加入适量KI溶液 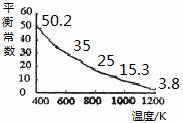
由于碘的挥发性较大,故不宜以直接法制备标准溶液 标定I2溶液的常用基准试剂是Na2C2O4 I2应先溶解在浓KI溶液中,再稀释至所需体积 标定I2溶液的常用基准试剂是As2O3
配制溶液时,只能用水作溶剂 配制硝酸铵溶液的过程中,溶液的温度会下降 用浓硫酸配制稀硫酸时,应将水缓缓注入浓硫酸中 将10g氯化钠溶于100g水中,得到质量分数为10%的氯化钠溶液
若a极变红,则在Pt电极上:2I--2e-===I2,淀粉遇碘变蓝 若b极变红,则在Pt电极上:4OH--4e-===2H2O+O2↑,O2将I.-氧化为I2,淀粉遇碘变蓝 若a极变红,则在Cu电极上:2Cu+4I--4e-===2CuI↓+I2,碘遇淀粉变蓝 若b极变红,则在Cu极上:Cu-2e-===Cu2+,Cu2+显蓝色
碘溶于浓碘化钾溶液中 碘直接溶于蒸馏水中 碘溶解于水后,加碘化钾 碘能溶于酸中
碘溶于40%碘化钾溶液中 碘直接溶于蒸馏水中 碘溶解于水后,加碘化钾 碘溶于酸性中
配制溶液时,只能用水作溶剂 配制硝酸铵溶液的过程中,溶液的温度会下降 用浓硫酸配制稀硫酸时,应将水缓缓注入浓硫酸中 将10 g氯化钠溶于100 g水中,得到质量分数为10%的氯化钠溶液
该反应的正反应是吸热反应 A.点与 点的化学反应速率vACC.在反应进行到 点时,v正>v逆D.A.点与B.点相比,B.点的c(I2)大
向上述体系中加入CCl4,平衡不移动 25 C时,向上述体系中加入少量I2,平衡向右移动, 平衡常数大于680 该反应的平衡常数表达式为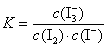 该反应的正反应为放热反应
该反应的正反应为放热反应
该反应的正反应是吸热反应 A.点与 点的化学反应速率vACC.在反应进行到 点时, v正逆D.A.点与B.点相比,B.点的c(I2)大
使用碘量瓶 溶液酸度控制在PH>8 适当加热增加I2的溶解度,减少挥发 加入过量KI

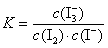 该反应的正反应为放热反应
该反应的正反应为放热反应

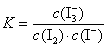 该反应的正反应为放热反应
该反应的正反应为放热反应