你可能感兴趣的试题
某二元弱酸的酸式盐NaHA溶液中:c(H+)十c(Na+)= c(OH-)+c(HA-)+c(A2-) 一定量的(NH4)2SO4与NH3・H2O混合所得的碱性溶液中:c(NH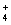 )>2c(SO
)>2c(SO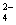 ) 在物质的量浓度均为0.01mol/L.的CH3COOH和CH3COONa的混合溶液中:c(CH3COOH)+c(CH3COO-)= 0.01mol/L. 相同温度下物质的量浓度相等的NH4HSO4溶液、NH4HCO3溶液、NH4Cl溶液中c(NH
) 在物质的量浓度均为0.01mol/L.的CH3COOH和CH3COONa的混合溶液中:c(CH3COOH)+c(CH3COO-)= 0.01mol/L. 相同温度下物质的量浓度相等的NH4HSO4溶液、NH4HCO3溶液、NH4Cl溶液中c(NH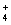 ):c(NH4HSO4)> c(NH4HCO3)> c(NH4Cl)
):c(NH4HSO4)> c(NH4HCO3)> c(NH4Cl)
该混合液中一定含有:K+、NH4+、CO32-、SO42-,可能含Cl- 该混合液中—定含有:NH4+、CO32-、SO42-,可能含K+、Cl- 该混合液中一定含有:NH4+、CO32-、SO42-、Cl-,可能含K+ 该混合液中:c(K+) ≥ 0.02mol/L c(CO32-) = 0.02mol/L
(2b-4c)/a mol/L (b-2c)/a mol/L (2b-c)/a mol/L (b-4c)/a mol/L
向0.1 mol/L的CH3COOH溶液中加入少量CH3COONH4固体,溶液的pH增大 室温下,pH=4的NaHSO4溶液中,水电离出的H+浓度为1×10﹣10mol/L 浓度均为0.1 mol/L的HCN溶液和NaCN溶液等体积混合(忽略体积变化),溶液中c(HCN)+c(CN﹣)=0.1 mol/L pH相同的①NH4Cl、②NH4Al(SO4)2、③(NH4)2SO4三种溶液的c(NH4+):②<③<①
(2b-4c)/amol/L (b-2c)/amol/L (2b-c)/amol/L (b-4c)/amol/L
向明矾溶液中加入等物质的量的Ba(OH)2溶液 Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O. 向Fe2(SO4)3溶液中通入足量的H2S. Fe3++H2S=Fe2++S↓+2H+ 向硝酸银溶液中滴加过量氨水 Ag++2NH3·H2O=[Ag(NH3)2]++2H2O. 含等物质的量的硫酸氢铵与氢氧化钠两种溶液混合: NH4++HSO4-+2OH-=SO42-+NH3↑+2H2O.
高锰酸钾完全分解后的残留物 洁净的食盐水 冰、水混合物 含氮30%的硝酸铵(NH4NO3)
NH4HCO3 (NH4)2SO4 NH4Cl CO(NH2)2
10mL 1mol/L (NH4)2SO4溶液 50mL 0.2mol/L NH4Cl溶液 10mL0.2mol/L(NH4)2SO4溶液 200mL 0.1mol/L NH4NO3溶液
0.01mol/L NH4Al(SO4)2溶液与0.02 mol/LBa(OH)2溶液等体积混合产生沉淀: NH4++Al3++2SO42−+2Ba2++4OH−=2BaSO4↓+ Al(OH)3↓+NH3·H2O NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O 向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀: 2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O 向FeCl3溶液中加入Na2S溶液产生沉淀:2Fe3++3S2-+6H2O=2Fe(OH)3↓+3H2S↑
CaCl2、NaOH、KNO3、Mg(NO3)2 FeCl3、H2SO4、KCl、NaNO3 NaHCO3、KCl、NH4NO3、Na2SO4 Mg(NO3)2、Na2SO4、NH4Cl、KNO3
可用Ba(OH)2溶液鉴别(NH4)2CO3、(NH4)2SO4、NH4NO3三种氮肥 MgCl2溶液、NaOH溶液、H2SO4溶液、CuSO4溶液,不加任何试剂即可鉴别 Na2CO3溶液、Ca(OH)2溶液、盐酸、BaCl2溶液,不加任何试剂即可鉴别 CuO粉末、炭粉、铁粉,三种黑色粉末用一种试剂无法鉴别

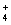 )>2c(SO
)>2c(SO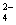 ) 在物质的量浓度均为0.01mol/L.的CH3COOH和CH3COONa的混合溶液中:c(CH3COOH)+c(CH3COO-)= 0.01mol/L. 相同温度下物质的量浓度相等的NH4HSO4溶液、NH4HCO3溶液、NH4Cl溶液中c(NH
) 在物质的量浓度均为0.01mol/L.的CH3COOH和CH3COONa的混合溶液中:c(CH3COOH)+c(CH3COO-)= 0.01mol/L. 相同温度下物质的量浓度相等的NH4HSO4溶液、NH4HCO3溶液、NH4Cl溶液中c(NH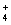 ):c(NH4HSO4)> c(NH4HCO3)> c(NH4Cl)
):c(NH4HSO4)> c(NH4HCO3)> c(NH4Cl)